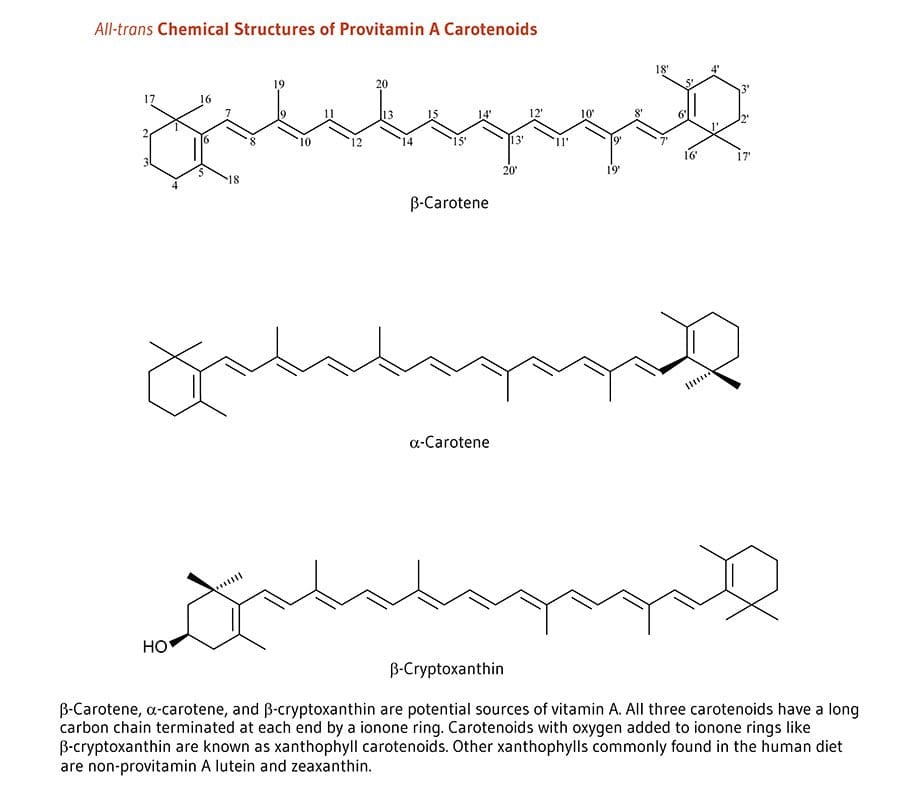
Resumo de Psoríase
A psoríase é um distúrbio imunológico comum, mediado por células T, caracterizado por placas circunscritas, avermelhadas e espessadas, com uma escala branca-prata sobrejacente. Ocorre em todo o mundo, embora a incidência seja menor em climas mais quentes e ensolarados. A principal causa da psoríase é desconhecida. Durante um estado de doença ativa, um mecanismo inflamatório subjacente é frequentemente envolvido. Muitos tratamentos convencionais concentram-se na supressão dos sintomas associados à psoríase e têm efeitos colaterais significativos. Este artigo analisa várias das abordagens naturais pesquisadas para o tratamento da psoríase, enquanto aborda a causa subjacente. (Rev Med 2007; 12 (4): 319-330)
Introdução
Avanços genéticos e imunológicos recentes aumentaram muito a compreensão da patogênese da psoríase como uma doença inflamatória imunomediada crônica. O defeito imunológico primário na psoríase parece ser um aumento na sinalização celular via quimiocinas e citocinas que atuam na expressão gênica regulada positivamente e causam hiperproliferação de queratinócitos. Uma nova compreensão desta doença complexa catalisou o desenvolvimento de tratamentos biológicos direcionados. No entanto, essas terapias revolucionárias não são isentas de riscos potenciais. Uma revisão das terapias naturais alternativas fornece algumas opções para aumentar a segurança e a eficácia no tratamento da psoríase. Psoríase Fisiopatologia, abordagens convencionais e alternativas para o tratamento Michael Traub, ND, e Keri Marshall MS, ND
Epidemiologia
A prevalência da psoríase varia muito, dependendo da etnia. A psoríase ocorre mais comumente em caucasianos, com uma ocorrência estimada de casos 60 por 100,000 / ano nesta população. Sua prevalência nos Estados Unidos é 2-4 por cento, embora seja rara ou ausente em nativos americanos e em certas populações afro-americanas. Embora comum no Japão, é muito menos comum na China, com uma incidência estimada de 0.3 por cento. A prevalência na população geral do norte da Europa e na Escandinávia é de 1.5-3 por cento. Mulheres e homens são igualmente afetados por essa condição. A observação de que a latitude afeta a prevalência provavelmente está relacionada ao efeito benéfico da luz solar sobre a doença.1 Embora a psoríase possa ocorrer em qualquer idade, a idade média de início da psoríase em placa é estimada em 33 anos, com 75 por cento dos casos iniciados antes da idade 46.2 A idade de início parece ser ligeiramente mais precoce nas mulheres do que nos homens. Estudos longitudinais sugerem que remissão espontânea pode ocorrer em cerca de um terço dos pacientes com psoríase.3
Fisiopatologia
Até recentemente, a psoríase era considerada um distúrbio dos queratinócitos epidérmicos; no entanto, agora é reconhecido principalmente como um distúrbio mediado pelo sistema imunológico. Para compreender adequadamente a disfunção imunológica presente na psoríase, é fundamental compreender a resposta imunológica normal da pele. A pele é um órgão linfóide primário com um sistema de vigilância imunológica eficaz equipado com células apresentadoras de antígeno, queratinócitos sintetizadores de citocinas, células T epidermotrópicas, células endoteliais capilares dérmicas, nódulos de drenagem, mastócitos, macrófagos de tecido, granulócitos, fibroblastos e células não Langerhans. A pele também possui linfonodos e linfócitos T circulantes. Juntas, essas células se comunicam por meio da secreção de citocinas e respondem de acordo com a estimulação por bactérias, produtos químicos, luz ultravioleta (UV) e outros fatores irritantes. A citocina primária liberada em resposta à apresentação do antígeno é o fator de necrose tumoral alfa (TNF-?). Geralmente, este é um processo controlado, a menos que o insulto à pele seja prolongado, caso em que a produção desequilibrada de citocinas leva a um estado patológico como a psoríase.
O debate continua se a psoríase é uma doença auto-imune ou uma disfunção imunológica T-helper 1 (Th1). Ativação de células T, TNF-? E células dendríticas são fatores patogênicos estimulados em resposta a um fator desencadeante, como lesão física, inflamação, bactéria, vírus ou retirada de medicação corticosteroide. Inicialmente, as células dendríticas imaturas na epiderme estimulam as células T dos nódulos linfáticos em resposta a uma estimulação de antígeno ainda não identificada. O infiltrado linfocítico na psoríase é predominantemente de células T CD4 e CD8. As moléculas de adesão que promovem a adesão de leucócitos são altamente expressas em lesões psoriáticas.4 Após as células T receberem estimulação e ativação primárias, ocorre uma síntese resultante de mRNA para interleucina-2 (IL-2), resultando em um aumento subsequente nos receptores de IL-2. A psoríase é considerada uma doença Th1 dominante devido ao aumento de citocinas da via Th1 interferon gama (IFN-?), IL-2 e interleucina 12 (IL-12) encontradas nas placas psoriáticas.
O aumento de IL-2 de células T ativadas e IL-12 de células de Langerhans, em última análise, regulam genes que codificam para a transcrição de citocinas, como IFN- ?, TNF-? E IL-2, responsáveis pela diferenciação, maturação e proliferação de Células T em células efetoras de memória. Por fim, as células T migram para a pele, onde se acumulam ao redor dos vasos sanguíneos dérmicos. Essas são as primeiras de uma série de alterações imunológicas que resultam na formação de lesões psoriáticas agudas. Como a resposta imune descrita acima é uma resposta um tanto normal à estimulação do antígeno, não está claro por que a ativação das células T que ocorre, seguida pela subsequente migração de leucócitos para a epiderme e derme, cria uma proliferação celular acelerada. A regulação gênica sobre-regulada pode ser um fator causal. O fator de crescimento endotelial vascular (VEGF) e a interleucina-8 liberados dos queratinócitos podem contribuir para a vascularização observada na psoríase.5
As células dendríticas parecem estar envolvidas na patogênese da psoríase. Um tipo de célula dendrítica envolvida são as células de Langerhans, a sentinela mais externa do sistema imunológico que reconhece e captura antígenos, migra para os linfonodos locais e os apresenta às células T. A ativação de linfócitos T libera citocinas pró-inflamatórias, como TNF-? que levam à proliferação de queratinócitos. Esta resposta hiperproliferativa diminui o tempo de trânsito epidérmico (o tempo aproximado que leva para a maturação normal das células da pele) de 28 dias para 2-4 dias e produz as placas eritematosas escamosas típicas da psoríase. Essa compreensão dos mecanismos patogênicos levou ao desenvolvimento e uso terapêutico do TNF-? agentes bloqueadores.
Cerca de 30 por cento dos indivíduos com psoríase têm história familiar da doença em um parente de primeiro ou segundo grau. Pelo menos nove loci de suscetibilidade cromossômica foram elucidados (PSORS1-9). HLA-Cw6 é o principal determinante da expressão fenotípica. Uma associação com o PSORS foi encontrada com polimorfismos funcionais em genes modificadores que medeiam a inflamação (por exemplo, TNF-?) E o crescimento vascular (por exemplo, VEGF) .6
Sabe-se que a psoríase se desenvolve em receptores de transplante de medula óssea de doadores com psoríase, desaparece em receptores de doadores sem psoríase e que os medicamentos imunossupressores são eficazes na redução da psoríase.7,8 Dada a predisposição genética para esta doença, o que pode ser feito para reduzir a expressão genética além de recorrer a terapias imunossupressoras? Uma abordagem naturopática consiste na modificação da dieta, jejum terapêutico, suplementação com omega-3, medicamentos naturais tópicos, fitoterapia e controle do estresse.
Pizzorno e Murray propõem que os supracitados antígenos não identificadosident resultam de digestão proteica incompleta, aumento da permeabilidade intestinal e alergias alimentares; intestino toxemia (endotoxinas); desintoxicação hepática prejudicada; deficiências de ácidos biliares; consumo de álcool; consumo excessivo de gorduras animais; deficiências nutricionais (vitaminas A e E, zinco e selênio); e estresse.9 Essas hipóteses, embora plausíveis, não foram adequadamente testadas.
Co-morbidades
A psoríase está associada a várias comorbidades, incluindo diminuição da qualidade de vida, depressão, aumento do risco cardiovascular, diabetes mellitus tipo 2, síndrome metabólica, câncer, doença de Crohn e artrite psoriática. Ainda não está claro se os cânceres, em particular o câncer de pele e o linfoma, estão relacionados à psoríase ou ao seu tratamento. A fototerapia e a terapia imunossupressora podem aumentar o risco de câncer de pele não melanoma, por exemplo.10
Particularmente preocupante é a ligação observada entre psoríase e doença cardiovascular. Evidências indicam que a psoríase é um fator de risco independente para doença cardiovascular.11 Dislipidemia, calcificação coronariana, aumento da proteína C reativa altamente sensível (PCR), folato diminuído e hiper-homocisteinemia são encontrados com frequência significativamente maior em pacientes com psoríase.12 Inflamação é o tema comum subjacente a ambas as condições, caracterizada pela presença de citocinas pró-inflamatórias e ativação endotelial.
Os processos inflamatórios subjacentes à psoríase também sugerem a possibilidade de deficiências de ácido graxo ômega-3, folato e vitamina B12, que também são freqüentemente encontradas em doenças cardiovasculares.13 Elevados níveis de homocisteína e de folato diminuídos se correlacionam com o Índice de Área e Gravidade da Psoríase (PASI). Uma rápida taxa de renovação das células da pele na psoríase pode resultar no aumento da utilização de folato e subsequente deficiência.14 O autor de um estudo conclui: A suplementação dietética de ácido fólico, B6 e B12 parece razoável em pacientes com psoríase, particularmente aqueles com homocisteína elevada, baixa folato e fatores de risco cardiovascular adicionais. 15
A artrite psoriática é uma condição clínica que ocorre em 25 por cento dos indivíduos atingidos pela psoríase.16 Em aproximadamente 10 por cento desta população, os sintomas artríticos precedem as lesões da pele. A artrite psoriática apresenta-se frequentemente como artrite inflamatória soronegativa, com uma apresentação clássica que consiste em oligoartrite, envolvimento da articulação interfalângica distal, dactilite (inflamação dos dígitos) e inflamação do calcâneo.
As opiniões conflitam se a condição da pele e a artrite representam uma manifestação diferente da mesma doença. Evidências genéticas, estudos imunológicos e variabilidade da resposta ao tratamento sugerem que eles podem ser duas condições diferentes, talvez com inflamação subjacente semelhante e irregularidade imune.17,18
Embora a pustulose palmoplantar (PP) seja frequentemente descrita como um subtipo de psoríase, diferentes dados demográficos e análises genéticas sugerem uma etiologia diferente da psoríase. Na aparência, o PP tem pústulas estéreis amareladas que aparecem nas palmas das mãos e nas solas dos pés. Apenas 25 por cento dos afetados relatam psoríase crônica em placas. PP ocorre com mais frequência em mulheres (9: 1 / feminino: masculino) e 95 por cento das pessoas afetadas têm uma história atual ou anterior de fumar. Como resultado, a PP pode ser considerada uma condição de comorbidade, em vez de uma forma distinta de psoríase.19
Critério de diagnóstico
A psoríase é classificada em vários subtipos, com a forma de placa crônica (psoríase vulgar) compreendendo aproximadamente 90 por cento dos casos. Placas escalonadas eritematosas e de demarcação acentuada ocorrem mais comumente na superfície extensora das regiões dos cotovelos, joelhos, couro cabeludo, sacro e virilha. Outras áreas envolvidas incluem as orelhas, a glande do pênis, a região perianal e os locais de trauma repetido. Um caso inflamatório ativo de psoríase pode demonstrar o fenômeno de Koebner no qual novas lesões se formam em um local de trauma ou pressão.
No futuro, a psoríase crônica em placas pode consistir em várias condições relacionadas com características fenotípicas e genotípicas distintas, fornecendo uma explicação para sua resposta variável à terapia, especialmente com agentes biológicos.
A psoríase inversa ocorre em locais intertriginosos e dobras cutâneas e é vermelha, brilhante e geralmente sem descamação. A sebopsoríase, que muitas vezes é confundida com dermatite seborreica, é caracterizada por escamas oleosas nas sobrancelhas, sulcos nasolabiais e áreas postauricular e pré-esternal.
A psoríase gutata aguda ocorre em crianças, adolescentes e adultos jovens, aproximadamente duas semanas após uma infecção aguda por estreptococos beta-hemolíticos, como amigdalite ou faringite, ou uma infecção viral. Ela se manifesta como uma erupção papular, eritematosa, com lesões menores que 1 cm de diâmetro no tronco e nas extremidades. A psoríase gutata aguda é geralmente autolimitada, resolvida nos meses 3-4. Um estudo indicou que apenas um terço dos indivíduos com psoríase gutata desenvolvem psoríase em placas clássica. 20
A psoríase pustulosa (von Zumbusch) também é uma erupção psoriásica aguda. O paciente apresenta febre e pústulas pequenas, monomórficas, dolorosas e estéreis, muitas vezes precipitadas por uma infecção intercorrente ou a retirada abrupta de esteróides tópicos sistêmicos ou superpotentes. Pode ser localizada nas palmas das mãos e plantas dos pés (psoríase palmar-plantar) ou pode ser generalizada e potencialmente fatal.
A psoríase eritrodérmica, também com risco de vida, envolve toda a superfície do corpo e pode resultar em hipotermia, hipoalbuminemia, anemia, infecção e insuficiência cardíaca de alto débito.
A doença da unha psoriática ocorre em aproximadamente 50 por cento dos pacientes com psoríase e manifesta-se mais comumente como picada. Outras alterações nas unhas podem incluir onicólise, descoloração, espessamento e distrofia.
Fatores de Risco
O desenvolvimento da psoríase envolve a interação de múltiplos fatores de risco genéticos com fatores ambientais, como infecção estreptocócica beta-hemolítica, HIV, estresse e medicamentos (por exemplo, betabloqueadores e lítio). Como mencionado anteriormente, a deficiência de folato e vitamina B12 também pode predispor. Além disso, há evidências de que o alcoolismo, tabagismo, obesidade, diabetes mellitus tipo 2 e síndrome metabólica aumentam o risco de desenvolver psoríase.
Com a exceção do VEGF, não foram encontrados biomarcadores como preditores confiáveis da atividade da psoríase. A PCR, as moléculas de adesão solúveis e os receptores de citocinas solúveis têm sido investigados, mas não se correlacionam com a gravidade.21
Tratamento Convencional
O tratamento convencional da psoríase é baseado no grau de gravidade. O tratamento de psoríase leve e limitado inclui corticosteróides tópicos, alcatrão, antralina, calcipotrieno (um análogo da vitamina D3), tazaroteno (um retinóide) e fototerapia. Os médicos podem estabelecer expectativas realistas para a terapia, dando ao paciente o controle da doença sem esperar pela cura completa. Psoríase do couro cabeludo geralmente responde a xampus de ácido salicílico.
O UVB de banda estreita é menos eficaz, mas mais seguro que o psoraleno associado ao ultravioleta A (PUVA), que acarreta um aumento do risco de câncer de pele. A exposição ao sol é outra forma de fototerapia. A exposição aos raios ultravioleta reduz a apresentação do antígeno e afeta a sinalização celular, favorecendo o desenvolvimento de respostas imunes do T-helper 2 (Th2). Células de Langerhans apresentadoras de antígenos estão diminuídas tanto no número quanto na função.22
Uma combinação tópica de calcipotrieno e betametasona (Taclonex ) mostrou maior eficácia na psoríase grave do que a monoterapia com ambos isoladamente.23
A adesão do paciente deve ser considerada ao desenvolver um plano de tratamento. O uso de solução tópica menos confusa e preparações de espuma de corticosteroides tópicos e calcipotrieno (comparado a pomadas e cremes) pode melhorar a complacência.
O tratamento sistêmico da psoríase grave geralmente envolve o uso de retinóides orais, metotrexato, ciclosporina e agentes biológicos que podem afetar significativamente outros sistemas corporais.
O retinóide oral acitretina é teratogênico e é convertido em etretinato com a ingestão concomitante de álcool. O etretinato tem meia-vida mais longa e é mais teratogênico do que a acitretina. Pacientes do sexo feminino devem usar duas formas de controle de natalidade e não devem engravidar por pelo menos três anos após o tratamento. Devido à possível interação com anticoncepcionais orais, a erva de São João (Hypericum perfoliatum) deve ser evitada. Outros efeitos adversos incluem efeitos mucocutâneos, triglicerídeos elevados, alopecia e hepatite. O tratamento com acitretina requer monitoramento frequente de hemogramas, perfis metabólicos abrangentes e análise de urina. As estratégias para reduzir a toxicidade da acitretina incluem o uso intermitente, redução da dose de manutenção em dias alternados ou a cada três dias, tratamento combinado com PUVA ou calcipotrieno tópico, dieta com baixo teor de gordura, exercícios aeróbicos, suplementação de óleo de peixe e, como afirmado acima, evitar o álcool.
O metotrexato (MTX) é o agente sistêmico mais comumente usado para psoríase e, por estar disponível há 35 anos, a maioria dos dermatologistas se sente confortável com seu uso. O metotrexato inibe a diidrofolato redutase (resultando em uma deficiência de ácido fólico ativo) e induz a adenosina A1, um potente agonista antiinflamatório. Seu mecanismo de ação pode ser ainda mais complexo, evidenciado pelo fato de que a cafeína inibe os efeitos antiinflamatórios do MTX na artrite reumatoide, mas não na psoríase ou artrite psoriática.24 Os efeitos adversos graves mais comuns do MTX são mielossupressão e fibrose hepática. Embora a mielossupressão não ocorra com frequência, os pacientes em uso de MTX frequentemente relatam sintomas de dor de cabeça, fadiga e náusea. A suplementação de folato reduz a incidência de anemia megaloblástica, hepatotoxicidade e intolerância gastrointestinal. Embora o ácido fólico e o ácido folínico pareçam ser igualmente eficazes, o ácido fólico é mais custo-efetivo.25 No entanto, um recente estudo duplo-cego de 22 pacientes com psoríase estáveis em terapia de longo prazo com MTX revelou que o ácido fólico reduziu a eficácia do MTX no controle da psoríase . Os pacientes foram aleatoriamente designados para receber 5 mg / dia de ácido fólico ou placebo por 12 semanas. O PASI médio aumentou (piorou) no grupo de ácido fólico, de 6.4 no início do estudo para 10.8 em 12 semanas. No grupo de placebo, o PASI médio caiu de 9.8 no início do estudo para 9.2 em 12 semanas (p <0.05 para a diferença na mudança entre os grupos) .26
A ciclosporina, uma droga potente e tóxica, às vezes é considerada para casos não controlados com acitretina, PUVA ou MTX, mas é contraindicada em pacientes com função renal anormal, hipertensão mal controlada, disfunção hepática ou imunossupressão. O uso prolongado resulta inevitavelmente em dano renal. A pressão arterial e a monitorização da creatinina são essenciais.
Os agentes biológicos bloqueiam a ativação das células T e o TNF- ?. Alefacept (Amevive ) interfere na ativação das células T e reduz as células T CD 45 RO + circulantes. Esta droga é uma proteína de fusão do receptor Fc de IgG1 e LFA3 humanos, um ligante coestimulador, que interage com o CD2 na superfície das células T. As células CD4 devem ser monitoradas semanalmente durante o tratamento com este agente.
Efalizumab (Raptiva ) é um anticorpo humanizado para CD11 que interfere com o tráfico de células T em tecidos inflamados e impede a ativação de células T. Embora seja rapidamente eficaz, pode ocorrer rebote.
TNF-? os bloqueadores regulam negativamente a expressão gênica pró-inflamatória e revertem o fenótipo psoriático. O etanercept (Enbrel ) é uma proteína de fusão dirigida contra o TNF-? Solúvel. O infliximabe (Remicade ) é um anticorpo monoclonal quimérico de camundongo / humano contra o TNF-? Solúvel e ligado à célula, enquanto o adalimumabe (Humira ) é um anticorpo monoclonal humano contra o TNF- ?. Esses TNF-? os inibidores são administrados por injeção e têm sido associados à indução de vários fenômenos autoimunes. Gosta de TNF-? em si, TNF-? os inibidores podem ter atividades pró-inflamatórias e antiinflamatórias. Só porque um determinado agente bloqueia o TNF-?, Não necessariamente beneficia a psoríase. Se um paciente é geneticamente predisposto à superprodução de TNF-?, Bloqueá-lo pode não ser suficiente para produzir benefício.27 Possíveis riscos do TNF-? os bloqueadores incluem reativação da tuberculose latente, hepatotoxicidade, linfoma e insuficiência cardíaca congestiva.
Desafios que permanecem com os biológicos para a psoríase incluem: (1) a compreensão do mecanismo predominante na psoríase e na artrite psoriática; (2) compreender diferentes respostas dos pacientes à terapia; (3) predizer a resposta clínica antes ou no início da terapia; (4) desenvolvendo formulações orais, inaladas e tópicas; e (5) determinar se o tratamento altera o resultado a longo prazo.
O ácido fumárico é a terapia primária de psoríase na Alemanha. Diminui as citocinas dependentes das células T, mas não é tão eficaz quanto os outros tratamentos convencionais, e carrega um alto risco de toxicidade e intolerância gastrointestinal.
O fornecimento de terapias rotativas e combinadas aumenta a eficácia e diminui a toxicidade do tratamento. O futuro pode trazer terapia com células-tronco e terapias baseadas em genes, incluindo tratamentos antisense que inibem diretamente genes específicos da psoríase. No entanto, os efeitos adversos e a toxicidade dos tratamentos convencionais para a psoríase exigem tratamentos naturais mais seguros e eficazes que podem ser usados como alternativas ou de forma integrativa.
Tratamentos naturais para a psoríase
Dieta
Uma abordagem baseada em evidências sugere que a psoríase, essencialmente um distúrbio inflamatório, deve se beneficiar de uma dieta anti-inflamatória, identificação, eliminação e / ou rotação de alimentos alergênicos e jejum terapêutico.28-30 Embora não haja dados publicados sobre evitação de alergia alimentar Muitos pacientes com psoríase apresentam sensibilidade aumentada ao glúten e seus sintomas de psoríase melhoram com uma dieta isenta de glúten.31 A medição de anticorpos para transglutaminase tecidual e gliadina pode ajudar a identificar este subgrupo. As evidências também sugerem que manter um peso saudável beneficia os pacientes com psoríase, uma vez que a psoríase correlaciona-se positivamente com o aumento do índice de massa corporal.32
O equilíbrio entre os eicosanóides pró-inflamatórios e antiinflamatórios é influenciado em grande parte pelo tipo de ácidos graxos consumidos na dieta. Uma dieta antiinflamatória consiste basicamente em uma ênfase em gorduras boas (peixes de água fria, nozes, sementes, azeite de oliva, outros óleos de alta qualidade), grãos inteiros, legumes, vegetais e frutas e na prevenção de gorduras ruins (saturadas gorduras animais, gorduras trans, alimentos fritos e processados, óleos de má qualidade) e carboidratos refinados. Além disso, uma quantidade excessiva de ácidos graxos ômega-6 na dieta pode contribuir para uma resposta inflamatória.33 As fontes primárias de óleos ômega-6 na dieta são óleos vegetais, como milho, soja, cártamo e girassol, enquanto as fontes primárias de ácido araquidônico são carne, ovos e laticínios.
A prostaglandina E2 (PGE2) é um eicosanóide proeminente derivado do ácido araquidônico de ácido graxo ômega-6. Uma ação dominante da PGE2 como uma molécula mensageira é aumentar a sensibilidade nos neurônios da dor, aumentar o inchaço e contrair os vasos sanguíneos. O consumo excessivo de óleos ômega-6 fornece substrato em excesso para a síntese de PGE2, que leva a uma resposta inflamatória agressiva e sustentada. Prostaglandina E3 (PGE3) é derivado do ácido graxo ômega-3, ácido eicosapentaenóico (EPA). Níveis mais elevados de PGE3 reduzem a sensibilidade à dor, relaxam os vasos sanguíneos, aumentam o fluxo sanguíneo e apoiam a resposta antiinflamatória natural do corpo (Figura 1).
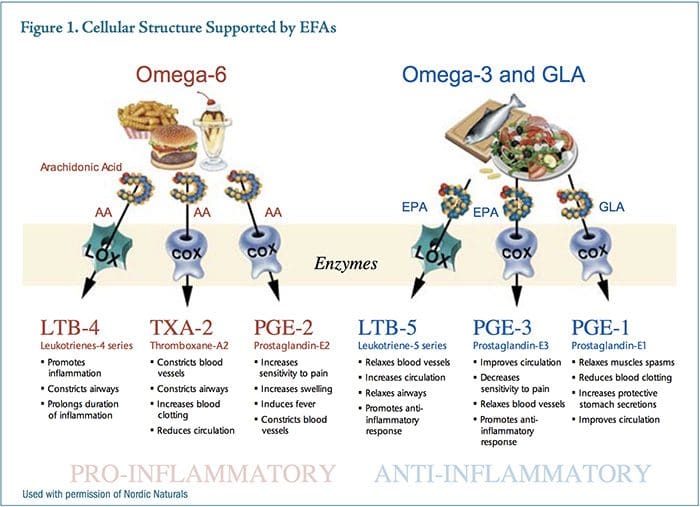
Embora tanto o PGE2 quanto o PGE3 sejam necessários para a homeostase adequada, as quantidades relativas dessas moléculas mensageiras competidoras contribuem ou mitigam síndromes inflamatórias crônicas. Acredita-se que a EPA atue competindo com o ácido araquidônico pelos sítios de ligação da ciclooxigenase-2 (COX-2), produzindo um mediador inflamatório menos potente, reduzindo, portanto, a inflamação.34
Antes da Revolução Industrial, não havia fontes significativas de óleos vegetais omega-6 na dieta. A maioria das culturas consumia dietas com baixo teor de óleos e alta em peixes ou carne bovina ou bisão de maior alcance em ômega-3s, criando uma proporção de ômega-6: ômega-3 que era aproximadamente 3: 1. A Revolução Industrial trouxe consigo o conhecimento e as ferramentas para refinar os óleos vegetais, resultando em uma rápida mudança nos hábitos alimentares da maioria das culturas ocidentais. A proporção de ômega-6: ômega-3 foi rapidamente empurrada para a atual estimativa de 11: 1: O corpo humano não foi capaz de se adaptar geneticamente a essa dramática mudança no consumo de ácidos graxos.
Muitas culturas modernas consomem grandes quantidades de óleos vegetais, principalmente em alimentos processados. Por exemplo, a produção de óleo de soja para consumo de alimentos aumentou 1,000 vezes entre 1909 e 1999.36 Além disso, o gado, aves e peixes de criação estão sendo alimentados com fubá e ração à base de soja, o que aumenta o conteúdo de carne e peixe. Quando os animais da fazenda são criados em grama, vermes ou outras dietas naturais, os tecidos são naturalmente mais ricos em ácidos graxos ômega-6.3
A indústria da carne apregoa marmorização em produtos acabados de carne bovina, que se deve à ração de milho e soja. O gado alimentado com milho e soja tem um teor de ácidos graxos ômega-6 mais alto em comparação com o gado alimentado com pasto. Enquanto o gado alimentado com pasto pode conter até 4 por cento de ácidos graxos ômega-3, o gado alimentado com milho normalmente contém 0.5 por cento de ômega-3
A dieta americana padrão fornece uma proporção média de ômega-6: ômega-3 de aproximadamente 11: 1. Uma dieta vegetariana pode colocar um indivíduo em risco decomer quantidades elevadas de óleos vegetais e produtos de soja e quantidades baixas de peixe, o que pode levar a balança a um estado pró-inflamatório. A redução de óleos vegetais na dieta e o aumento das gorduras omega-3 EPA e ácido docosahexaenóico (DHA) por meio do consumo de peixes gordurosos, como bacalhau, salmão, cavala e sardinha, podem beneficiar indivíduos que sofrem de condições inflamatórias crônicas.33
Várias ervas usadas como temperos, incluindo cúrcuma, pimenta vermelha, cravo, gengibre, cominho, erva-doce, erva-doce, manjericão, alecrim, alho e romã, podem bloquear a ativação do fator nuclear kappaB (NF? B) de citocinas inflamatórias.38
Abordagens dietéticas que modificam a ingestão de ácidos graxos podem influenciar o perfil de eicosanóides de forma que processos inflamatórios como a produção de ácido araquidônico e ativação de células T sejam atenuados, enquanto citocinas como interleucina-4 (a principal citocina responsável por estimular uma resposta imune Th2). ) são regulados para cima.34
Suplementação Nutricional
Ácidos Graxos Essenciais
Os ácidos graxos essenciais (EFAs) influenciam a fisiopatologia da psoríase de três maneiras: primeiro, os EFAs afetam a cinética das membranas celulares; segundo, os EFAs impactam o fluxo sanguíneo dérmico e epidérmico por meio da função endotelial aprimorada; e terceiro, os EFAs atuam como um agente imunomodulador por meio de seu impacto sobre os eicosanóides. Os EFAs são usados como substratos básicos no desenvolvimento da camada dupla de fosfolipídios em praticamente todas as células do corpo humano, incluindo a derme e a epiderme. Eles criam integridade estrutural que regula a fluidez, o que impacta o transporte celular, a ligação do mensageiro e a comunicação celular. Os ácidos graxos ômega-3 podem atuar direta e indiretamente na função endotelial, reduzindo citocinas de células mononucleares, como IL-1 e TNF ?, 39 diminuindo a formação de proteína quimio-atrativa fator de crescimento derivado de plaquetas (PDGF), aumentando a biodisponibilidade de óxido nítrico e reduzindo a expressão de moléculas de adesão. O efeito cumulativo que modula esses mediadores bioativos é evitar a vascularização ou o crescimento de novos vasos sanguíneos dentro da placa psoriática, ao mesmo tempo que permite uma melhor perfusão do tecido dérmico.
Os componentes da imunidade natural e adquirida, incluindo a produção dos principais moduladores imunológicos, podem ser afetados pela ingestão de ácidos graxos ômega-3 e -6, conforme discutido acima. Os efeitos imunomoduladores dos ácidos graxos ômega-3 incluem a supressão de linfoproliferação, células CD4 +, apresentação de antígenos, apresentação de moléculas de adesão, respostas de Th1 e Th2 e produção de citocinas pró-inflamatórias.34
Vários estudos demonstraram o benefício da suplementação intravenosa ou oral de óleo de peixe para a psoríase.40-42 Em um estudo realizado por Mayser et al, infusões intravenosas de ácidos graxos ômega-3 levaram a um aumento do leucotrieno anti-inflamatório B5 (LTB5) dentro de 4-7 dias de início do tratamento, quando comparados com pacientes controle.43 Neste estudo, os pacientes receberam uma preparação ômega-3 ou ômega-6 duas vezes ao dia por 10 dias. Não foram observados efeitos colaterais.
O EPA compete com o ácido araquidônico (AA) pela 5-lipoxigenase e produz o LTB5, que é apenas um décimo tão potente quanto o mediador inflamatório leucotrieno B4 (LTB4). Os níveis de LTB4 mostraram-se elevados nas placas psoriásicas e demonstram as propriedades quimiotáticas necessárias para a infiltração da proliferação de leucócitos e queratinócitos.43
O artigo de revisão de Ziboh sobre ômega-3 e psoríase faz referência a seis estudos conduzidos com suplementação oral de óleo de peixe com resultados mistos. Infelizmente, as referências originais não podem ser encontradas. Dois estudos foram duplo-cegos e controlados por placebo, usando 1.8 g de EPA e DHA ao longo de cursos de oito semanas e 12 semanas. O estudo de oito semanas demonstrou benefício em coceira, descamação e eritema, enquanto o estudo de 12 semanas não mostrou benefício.44
Três estudos abertos foram realizados, fornecendo 10-18 g EPA e DHA diariamente durante oito semanas. Todos os estudos mostraram melhora, com dois estudos demonstrando leve a moderado e um estudo demonstrando moderada a excelente melhora na escala, prurido e espessura da lesão. Um estudo aberto combinado com uma dieta com baixo teor de gordura mostrou uma redução significativa nos sintomas psoriásicos.44,45
Vários estudos exploraram o uso de óleo de peixe tópico em concentrações variáveis de EPA. Alguns estudos relataram benefícios, incluindo uma redução na espessura e escamação da placa.46,47 Em um estudo de Puglia et al, extratos de óleo de peixe e cetoprofeno foram aplicados topicamente a lesões psoriásicas, com uma redução observada no eritema.48 A desvantagem mais significativa para a aplicação tópica de óleo de peixe é a conformidade devido ao odor.
O óleo de peixe também provou ser benéfico em condições de articulação auto-imune, como a artrite reumatóide (RA) .49 Embora a suplementação de óleo de peixe não tenha sido usada em ensaios clínicos para o tratamento da artrite psoriática, pode ser benéfica no tratamento desta condição. muitas semelhanças com a AR, incluindo um mecanismo inflamatório subjacente comum e imune disfunção.
Folato
A terapia com metotrexato resulta em uma deficiência de folato. Como mencionado acima, em pacientes recebendo MTX para psoríase, a suplementação com folato reduziu a incidência de hepatotoxicidade e intolerância gastrointestinal, mas pode prejudicar a eficácia do MTX.24 Ao suplementar com ácido fólico ou as formas ativas, ácido folínico ou 5-metiltetrahidrofolato, a dose recomendada é 1-5 mg / dia.
Proteína Whey Bioativa Isolada
XP-828L é um novo suplemento dietético feito a partir de um extrato protéico derivado do soro de leite bovino que recentemente demonstrou ser benéfico na psoríase.50,51 O perfil bioativo do XP-828L é provavelmente devido à presença de fatores de crescimento, imunoglobulinas e ativos péptidos encontrados neste extracto específico de soro de leite. Um estudo in vitro demonstrou que o XP-828L tem efeitos reguladores imunológicos, incluindo a inibição da produção de citocinas Th1, tais como IFN-g e IL-2, o que pode torná-lo eficaz no tratamento de distúrbios relacionados com T-helper 1, como a psoríase. 52
Um estudo aberto foi conduzido em 11 pacientes adultos com psoríase em placas estável e crônica em dois por cento ou mais da área total de superfície corporal. Os participantes do estudo receberam 5 g duas vezes ao dia de XP-828L por 56 dias. As avaliações usando o PASI e os escores da Avaliação Global do Médico (PGA) foram feitas no dia da triagem inicial e novamente nos dias 1, 28 e 56. Na conclusão do estudo, sete dos 11 indivíduos tiveram uma pontuação PASI reduzida que variou de 9.5 por cento para 81.3 por cento.50 Os resultados de um duplo-cego maior, estudo controlado por placebo de 84 indivíduos com psoríase leve a moderada mostrou que XP-828L (5 g / dia por 56 dias) reduziu significativamente a pontuação PGA em comparação com placebo (p <0.05). Nenhum efeito adverso foi observado em nenhum dos participantes do estudo.50,51
A vitamina D
Foi estabelecido que os pacientes com psoríase disseminada diminuíram significativamente os níveis séricos da forma biologicamente ativa da vitamina D, 1-alfa, 25-dihidroxivitamina D3 (1 - ?, 25 (OH) 2D3; calcitriol) em comparação com a idade e o sexo -controles pareados e também em comparação com pacientes com psoríase moderada.53 Se isso é um fator que contribui para a psoríase ou um resultado do distúrbio, não foi elucidado.
Os queratinócitos na epiderme convertem o 7-desidrocolesterol em vitamina D3 na presença de UVB. Luz solar, fototerapia UVB, calcitriol oral e análogos de vitamina D tópica são terapia eficaz para psoríase devido às ações antiproliferativas e pró-diferenciadoras da vitamina D nos queratinócitos.54-56
A ligação do Calcitriol aos receptores da vitamina D (VDR) na pele modula a expressão de um grande número de genes, incluindo reguladores do ciclo celular, fatores de crescimento e seus receptores. Polimorfismos do gene VDR estão associados à psoríase e podem predispor ao desenvolvimento de psoríase e resistência à terapia com calcipotriol, bem como contribuir para a disfunção hepática em pacientes com psoríase.57
Dada a importância da vitamina D na psoríase, câncer, doenças inflamatórias e outras condições, foi sugerido por alguns pesquisadores que as recomendações para proteção solar e prevenção do câncer de pele podem precisar ser reavaliadas para permitir o status de vitamina D suficiente. Um estudo recente mostrou que a exposição abundante ao sol em uma amostra de adultos no Havaí não garantiu necessariamente a adequação de vitamina D, o que aponta para a necessidade de suplementação de vitamina D para atingir níveis sanguíneos ideais.58
Estudos demonstraram que a vitamina D oral pode ser tomada com segurança em doses diárias de até 5,000 UI, com alguns especialistas recomendando até 10,000 UI diariamente para corrigir uma deficiência.59-61 A administração oral e tópica de vitamina D, luz solar e UVB tem demonstrado eficácia considerável no tratamento da psoríase.56
Tratamentos tópicos da psoríase
Vários tratamentos tópicos para psoríase podem fornecer benefícios, incluindo calcipotrieno (Dovonex ; um análogo sintético da vitamina D3), Berberis aquifolium creme (10%) 62 (Psoriaflora ; Relieva ), gel de curcumina (1%), Aloe vera e um pomada rica em flavonóides (Flavsalve ).
O gel de curcumina produziu resolução de 90 por cento das placas em 50 por cento dos pacientes dentro de 2-6 semanas; o restante dos sujeitos do estudo mostraram melhora de 50 a 85 por cento. A curcumina foi considerada duas vezes mais eficaz do que o creme de calcipotriol (que geralmente leva três meses para exercer seu efeito total). O mecanismo da curcumina é como um inibidor seletivo da fosforilase quinase, reduzindo assim a inflamação por meio da inibição de NF? B.63
Um ensaio controlado de creme de extrato de Aloe vera (0.5%) em 60 pacientes por 4-12 meses demonstrou uma eliminação significativa das placas psoriáticas (82.8%) em comparação com o placebo (7.7%) (p <0.001). Além disso, o PASI diminuiu para uma média de 2.2.64
A escamação da psoríase se beneficia do uso de emolientes. Os lipídios intercelulares, como as ceramidas (moléculas de lipídios compostas por ácidos graxos e esfingosina), desempenham um papel importante na regulação da homeostase da barreira da água da pele e na capacidade de retenção de água. Foi demonstrado que as ceramidas estão diminuídas na epiderme psoriática. Emolientes mais novos contendo ceramida (por exemplo, CeraVe , Mimyx , Aveeno Eczema Care) mostraram benefícios na psoríase e podem melhorar a função de barreira da pele e diminuir a perda de água.65
Influências Botânicas
Uma fórmula à base de ervas chinesas (Herose Psoria Capsule) demonstrou segurança e eficácia no tratamento da psoríase em placas grave.66 A herose consiste em rizoma Zingiberis, radix Salviae miltiorrhizae, radix Astragali, ramulus Cinnamomi, radix Paeoniae alba, radix Codonopsis pilosulae sêmen Coicis. Em um ensaio clínico aberto, 15 indivíduos tomaram quatro cápsulas de Herose (450 mg cada) três vezes ao dia durante 10 meses. O investigador avaliou o PASI e a resposta terapêutica ao Herose para cada paciente. A fórmula tem como objetivo aquecer o yang e promover a circulação sanguínea.
Intervenções de estilo de vida
Fatores de estilo de vida como tabagismo e consumo de álcool estão associados à gravidade da psoríase.67 Atividade física e atividades ao ar livre (tomando precauções para não queimar) são benéficas.68 Tomar banho e tomar sol no Mar Morto por quatro semanas resultou em uma diminuição do PASI 81.5 por cento, uma diminuição de 78-percentual na hiperplasia dos queratinócitos, e quase total eliminação de linfócitos T da epiderme, com um baixo número remanescente na derme.69
O controle do estresse pode beneficiar indivíduos com psoríase. Os indivíduos que ouviram uma fita de meditação guiada durante a fototerapia tiveram uma melhora quatro vezes mais rápida do que aqueles que receberam apenas fototerapia, conforme julgado por dois dermatologistas independentes. O status da psoríase foi avaliado de três maneiras: inspeção direta por enfermeiras clínicas; inspeção direta por médicos cegos às condições do estudo do paciente (fita ou sem fita); e avaliação cega do médico de fotografias de lesões de psoríase. Quatro indicadores sequenciais do estado da pele foram monitorados durante o estudo: um primeiro ponto de resposta, um ponto de viragem, um ponto intermediário e um ponto de compensação. Os indivíduos nos grupos de fita atingiram o Ponto Médio (p = 0.013) e o Ponto de Clearing (p = 0.033) significativamente mais rapidamente do que aqueles na condição sem fita, para os tratamentos com UVB e PUVA.70 Finalmente, a psicoterapia pode ser essencial adjunto para indivíduos com problemas psicológicos não resolvidos persistentes, como ansiedade, depressão e estresse psicossocial desta doença crônica de pele.
Discussão
A psoríase é caracterizada pela ativação de células T que libera citocinas pró-inflamatórias como o TNF- ?, levando à proliferação de queratinócitos e às lesões cutâneas típicas da psoríase.
A abordagem convencional da psoríase consiste na utilização de corticosteroides tópicos e / ou orais, outras drogas imunossupressoras, retinoides orais, luz ultravioleta e vários (não necessariamente novos, já utilizados anteriormente para Crohn e AR) agentes biológicos. Embora esses tratamentos possam ser altamente eficazes no controle da doença, nenhum é universalmente seguro e eficaz, e cada um carrega um perfil de risco considerável.
Existem algumas evidências do uso de modificações dietéticas e de óleo de peixe para diminuir a inflamação na psoríase. Mais pesquisas são necessárias para esclarecer o uso destas e várias terapias botânicas tópicas e intervenções de estilo de vida para melhorar os sintomas clínicos, diminuindo a expressão fenotípica da psoríase e proporcionando tratamentos seguros e eficazes.