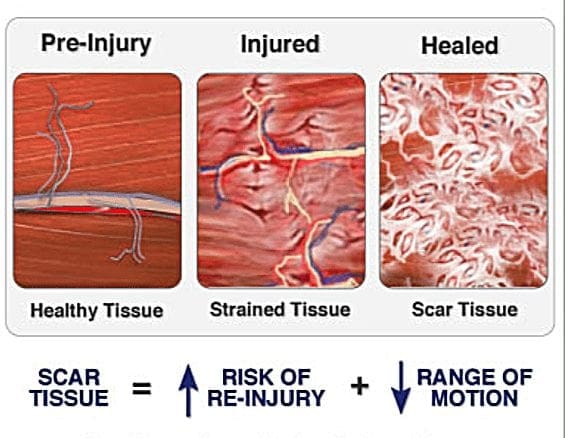
Mecanismos de caminho de modulação da dor em El Paso, TX
A maioria, se não todas, as doenças do corpo desencadeiam a dor. Dor é interpretado e sentido no cérebro. A dor é modulada por dois tipos principais de drogas que operam no cérebro: analgésicos e anestésicos. O termo analgésico refere-se a um medicamento que alivia a dor sem perda de consciência. A expressão anestesia central refere-se a um medicamento que deprime o SNC. Distingue-se pela falta de toda percepção de modalidades sensoriais, por exemplo, perda de consciência sem perda de funções críticas.
Analgesia do Ópio (AO)
Os fármacos clinicamente mais bem sucedidos para a produção de analgesia temporária e alívio da dor são a família de opióides, que inclui morfina e heroína. Atualmente, não há opções terapêuticas adicionais para os opiáceos. Vários efeitos colaterais causados pelo uso de opiáceos incluem tolerância e dependência de drogas ou dependência. Em geral, essas drogas modulam as informações de dor que chegam na coluna e no sistema nervoso central, além de aliviar a dor temporariamente, e também podem ser chamadas de analgesia produtora de opiáceos (OA). O antagonista de opiáceos é um fármaco que antagoniza os efeitos dos opiáceos, como a naloxona ou a maltroxona, etc. São antagonistas competitivos dos receptores de opiáceos. No entanto, o cérebro tem um circuito neuronal e substâncias endógenas que modulam a dor.
Opioides endógenos
A neurotransmissão opioidérgica localiza-se em todo o cérebro e medula espinhal e acredita-se que influencie muitas funções do sistema nervoso central, como nocicepção, funções cardiovasculares, termorregulação, respiração, funções neuroendócrinas, funções neuroimunes, consumo alimentar, atividade sexual, competição comportamento locomotor, bem como memória e aprendizagem. Os opioides exercem efeitos marcantes sobre o humor e a motivação e produzem uma sensação de euforia.
São identificadas três classes de receptores opióides:? -Mu,? -Delta e? -Kappa. Todas as 3 classes estão amplamente dispersas no cérebro. Os genes que codificam cada um deles foram clonados e funcionam como membros dos receptores da proteína G. Além disso, três tipos principais de péptidos opióides endógenos que interagem com os receptores opióides acima foram reconhecidos no sistema nervoso central, incluindo, <3> -endorfinas, encefalinas e dinorfinas. Esses 2 peptídeos opioides são derivados de um grande receptor de proteína por três genes diferentes, como o gene proopiomelanocortina, ou POMC, o gene da proencefalina e o gene da prodinorfina. Os peptídeos opioides modulam a entrada nociceptiva de duas maneiras: primeiro, eles bloqueiam o neurotransmissor liberados pela inibição do influxo de CaXNUMX + no terminal pré-sináptico, ou em segundo lugar, eles abrem os canais de potássio, que hiperpolariza os neurônios e inibe a atividade do pico. Eles agem em vários receptores no cérebro e na medula espinhal.
As encefalinas são consideradas os ligantes putativos para o? receptores,? endorfinas para seus receptores? e dinorfinas para os? receptores. Os vários tipos de receptores opióides são distribuídos de forma diferente no sistema nervoso periférico e central, ou SNC. Existem evidências de diferenças funcionais nesses receptores em várias estruturas. Isso explica por que muitos efeitos colaterais indesejáveis ocorrem após tratamentos com opiáceos. Por exemplo, os receptores mu (?) Estão disseminados nos núcleos parabraquiais do tronco cerebral, onde um centro respiratório e a inibição desses neurônios podem causar o que é conhecido como depressão respiratória.
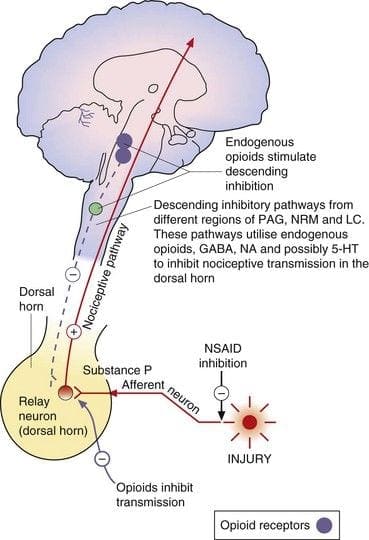
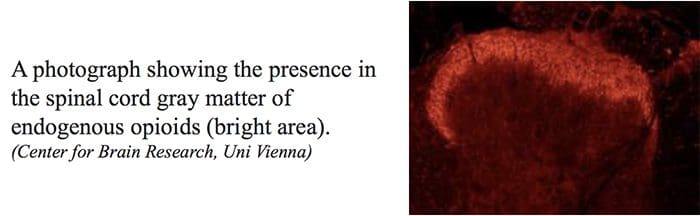
Os terminais centrais ou periféricos das fibras aferentes nociceptivas apresentam receptores opióides nos quais os opioides exógenos e endógenos poderiam atuar para modular a capacidade de transmitir informações nociceptivas. Além disso, altas densidades de receptores opiáceos são encontradas em cinza periaquedutal, ou PAG, núcleo magno da rafe ou NRM e rafe dorsal, ou DR, da medula rostral ventral, na medula espinhal, núcleo caudado ou CN, núcleo septal, hipotálamo, habenula e hipocampo. Os opioides administrados sistemicamente em doses analgésicas ativam os mecanismos espinhais e supraespinhais via?,? e? tipo receptores opióides e regular os sinais de dor para modular os sintomas.
Circuitos Neuronais e Modulação da Dor
Por muitas décadas, foi sugerido que em algum lugar do sistema nervoso central existe um circuito que pode modular os detalhes da dor que chega. A teoria do controle do portão e o sistema de transmissão da dor ascendente / descendente são duas sugestões de tal circuito. Abaixo, discutiremos mais detalhadamente.
Teoria do Controle de Portão
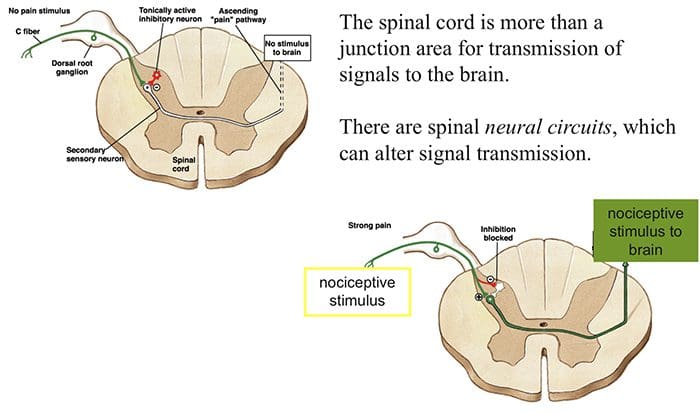
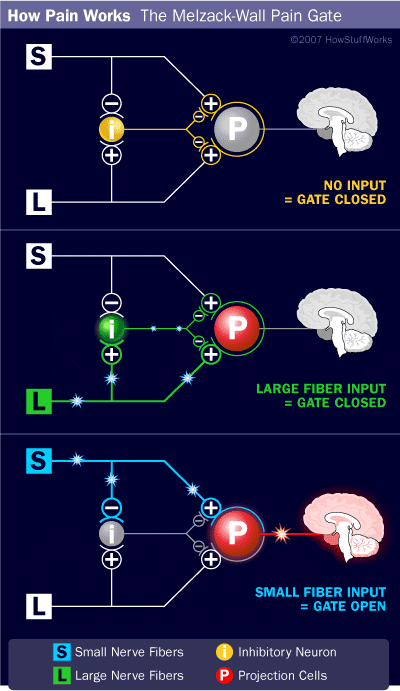
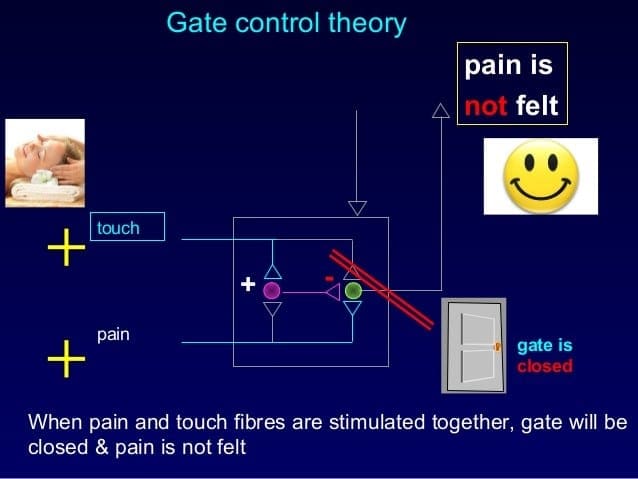
O mecanismo inicial de modulação da dor conhecido como teoria de controle de portão, foi proposto por Melzack e Wall em meados do 1960. A noção da teoria do controle do portão é que a entrada não dolorosa fecha os portões para entrada dolorosa, o que resulta em evitar a sensação de dor de viajar para o SNC, por exemplo, entrada não-nociva, ou estimulação, suprime a dor.
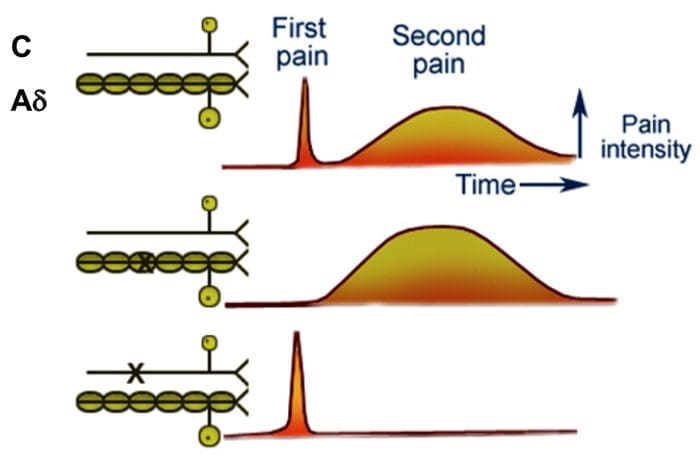
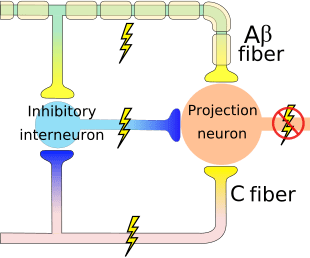
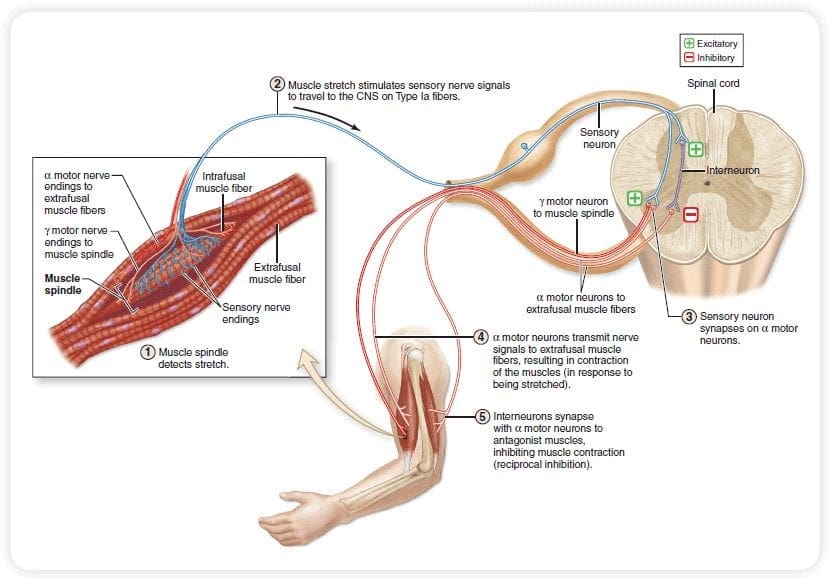
A teoria implica que os colaterais das grandes fibras sensoriais que transportam a entrada sensorial cutânea ativam os interneurônios inibitórios, os quais inibem e regulam os dados de transmissão da dor transportados das fibras da dor. Entrada não-nociva inibe a dor, ou entrada sensorial, e fecha o portão para entrada nociva. A teoria de controle do portão demonstra que, no nível da medula espinhal, a estimulação não-nociva criará inibição pré-sináptica nas fibras nociceptoras da raiz dorsal que fazem sinapse nos neurônios espinhal dos nociceptores (T). Esta inibição pré-sináptica também impedirá que a informação nociva de entrada chegue ao SNC, por exemplo, fechará a porta para a informação tóxica de entrada.
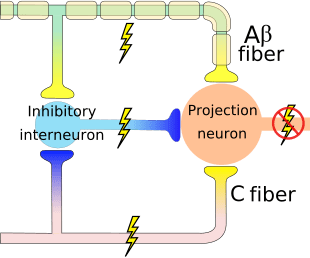
A teoria do controle do portão foi a razão para a idéia por trás da produção e utilização da estimulação elétrica nervosa transcutânea, ou TENS, para o alívio da dor. Para ser eficaz, a unidade TENS gera duas frequências diferentes abaixo do limiar de dor que podem ser tomadas pelo paciente. Este processo encontrou um grau de realização no tratamento da dor crônica.
Modulação da Dor: Teoria do Controle do Portão
Analgesia Produzida por Estimulação (SPA)
A evidência de um sistema de analgesia inerente foi encontrada pela estimulação elétrica intracraniana de certas regiões cerebrais discretas. Essas áreas seriam o cinza periaquedutal, ou PAG, e o núcleo rafe magha, ou NRM, rafe dorsal ou DR, núcleo caudado, ou CN, núcleo septal ou Spt, junto com outros núcleos. Tal estimulação ou sinais sensoriais, inibe a dor, produzindo analgesia sem supressão comportamental, enquanto a sensação de toque, temperatura e pressão permanece intacta. De acordo com estudos de pesquisa, SPA, ou estimulação produziu analgesia, é mais pronunciada e continua por um longo período de tempo após a estimulação em humanos do que em animais experimentais. Além disso, durante o SPA, os indivíduos, no entanto, ainda respondem à estimulação não dolorosa, como temperatura e toque, dentro da região circunscrita da analgesia. O mais efetivo sistema nervoso central (SNC), ou regiões do sistema nervoso central para a ocorrência do SPA, estaria no PAG e no núcleo da rafe, ou RN.
A estimulação elétrica de PAG ou NRM inibe as células tálmicas da coluna vertebral, ou neurônios espinhais que se projetam monossinapticamente ao tálamo, nas lâminas I, II e V para assegurar a informação nociva dos nociceptores que são modulados no nível da medula espinhal. Além disso, o PAG tem conexões neuronais com o núcleo rafe magnus ou NRM.
A atividade do PAG ocorre mais provavelmente pela ativação da via descendente da NRM e provavelmente também pela ativação de conexões ascendentes que atuam em níveis subcorticais maiores do SNC. Além disso, a estimulação elétrica de PAG ou NRM produz analgesia comportamental, ou a estimulação produziu analgesia. A estimulação produziu analgesia, ou o SPA causa a liberação de endorfinas que podem ser bloqueadas pelo antagonista opiáceo naloxona.
Durante a estimulação PAG e / ou RN, a serotonina, também conhecida como 5-HT, também pode ser descarregada dos axônios ascendentes e descendentes dos núcleos subcorticais, nos núcleos espinhais do trigêmeo e na medula espinhal. Esta liberação do 5-HT modula e regula a transmissão da dor, inibindo ou bloqueando a ação neural. A depleção de 5-HT por lesão elétrica dos núcleos da rafe ou com uma lesão neurotóxica causada por injeção local de um agente químico, como a paraclorofenilalanina, ou PCPA, resulta no bloqueio do poder do opiáceo, tanto intracraniano e sistêmico, quanto estimulação elétrica para produzir analgesia.
Para confirmar se a estimulação elétrica produziu analgesia via liberação de opiáceos e dopamina, então a região é localmente microinjetada com morfina ou 5-HT. Todas essas microinjeções acabam criando analgesia. Esses processos também fornecem uma maneira de identificar áreas cerebrais relacionadas à supressão da dor e ajudam a produzir um mapa dos centros de dor. A maneira mais eficaz de produzir analgesia por opiáceos, ou OA, é por injeção intracerebral de morfina no PAG.
O PAG e o RN, bem como outras estruturas cerebrais nas quais a analgesia é produzida, também são ricos em receptores de opiáceos. A administração intracerebral de opióides produziu analgesia e a SPA pode ser bloqueada por microinjeções sistêmicas ou locais de naloxona, o antagonista da morfina, na PAG ou RN. Por essa razão, tem sido sugerido que os dois, OA e SPA, operam por um mecanismo frequente.
Se OA e SPA se comportarem através do mesmo sistema intrínseco, então a hipótese de que os opiáceos ativam um mecanismo de supressão da dor é muito mais provável. De fato, as evidências atuais sugerem que as microinjeções de um opiáceo no PAG ativam um sistema tronco cerebral eferente que inibe a transmissão da dor nos níveis segmentares da medula espinhal. Estas observações implicam que a analgesia provocada pelo cinza periaquedutal, ou PAG, exige uma via descendente para a medula espinhal.

Insight do Dr. Alex Jimenez
A modulação da dor ocorre através do processo de estimulação cerebral elétrica que ocorre devido à ativação de fibras inibitórias descendentes, que regulam ou inibem a entrada e saída de certos neurônios. O que tem sido descrito como antagonistas opioides e serotoninérgicos, acredita-se que reverte a analgesia local por opiáceos e a analgesia gerada por estímulos cerebrais. Os sinais ou impulsos sensoriais no sistema nervoso central são controlados por sistemas inibitórios ascendentes e descendentes, utilizando opioides endógenos ou outras substâncias endógenas, como a serotonina como mediadores inibitórios. A dor é uma percepção complexa que também pode ser influenciada por uma variedade de outros fatores, incluindo o estado emocional.
Mecanismos de Modulação da Dor
Mecanismo de Supressão da Dor Ascendente e Descendente
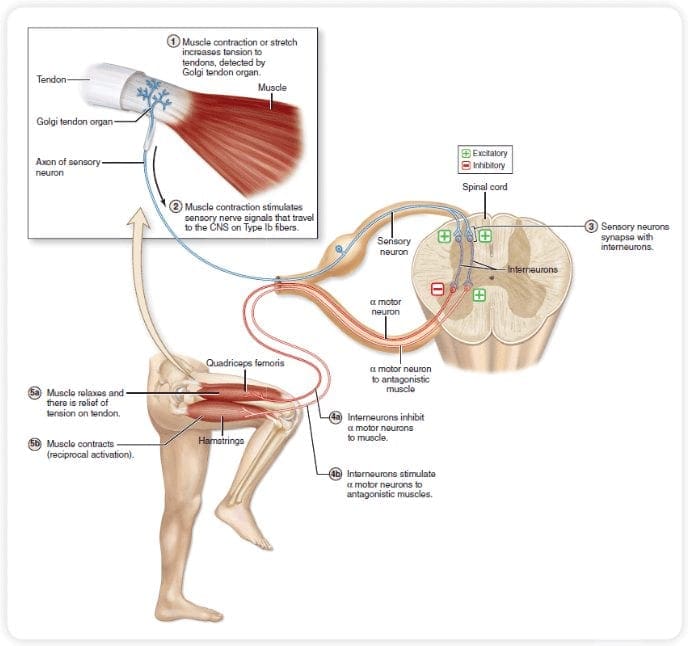
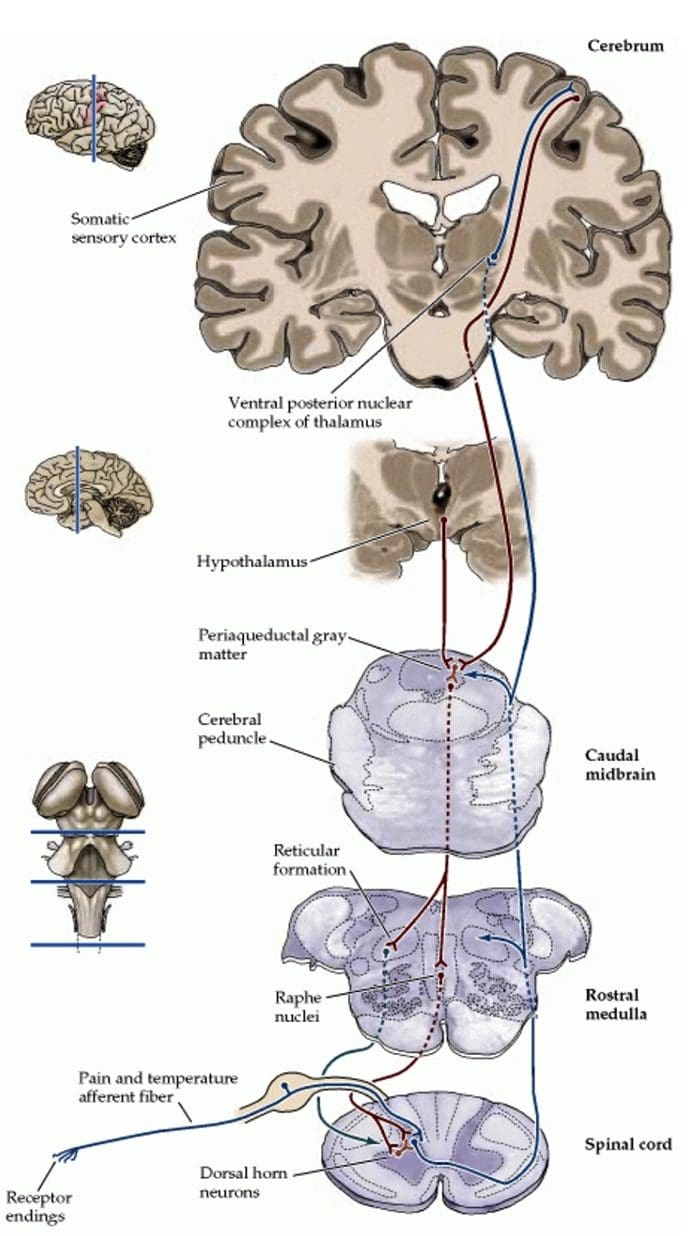
As fibras ascendentes primárias da dor, como o A? e fibras C, alcançam o corno dorsal da medula espinhal de áreas de nervos periféricos para inervar os neurônios nociceptores nas lâminas de Rexed I e II. As células da lâmina II de Rexed fazem conexões sinápticas nas camadas IV a VII de Rexed. As células, particularmente nas lâminas I e VII do corno dorsal, dão origem aos tratos espinotalâmicos ascendentes. No nível espinhal, os receptores opiáceos estão localizados nas terminações pré-sinápticas de seus nocineurônios e nas camadas do nível interneural IV a VII do corno dorsal.
A ativação de receptores opiáceos no nível interneuronal produz hiperpolarização dos neurônios, o que leva à inibição da ativação e também à liberação da substância P, um neurotransmissor envolvido na transmissão da dor, evitando assim a transmissão da dor. O circuito que consiste no cinza periaquedutal, ou PAG, matéria no tronco cerebral superior, o locus coeruleus, ou LC, o núcleo magno da rafe, ou NRM, e o núcleo reticularis gigantocelular, ou Rgc, leva à dor descendente via de supressão, que inibe a entrada de dados de dor no nível da medula espinhal.
Como afirmado anteriormente, os opioides interagem com os receptores opiáceos em níveis distintos do sistema nervoso central. Esses receptores opióides são regiões-alvo normais para hormônios e opiáceos endógenos, como as endorfinas e as encefalinas. Devido à ligação no receptor em sites subcorticais, mudanças secundárias que resultam em alguma mudança nas propriedades eletrofisiológicas dos neurônios e na regulação de suas informações de dor ascendente.
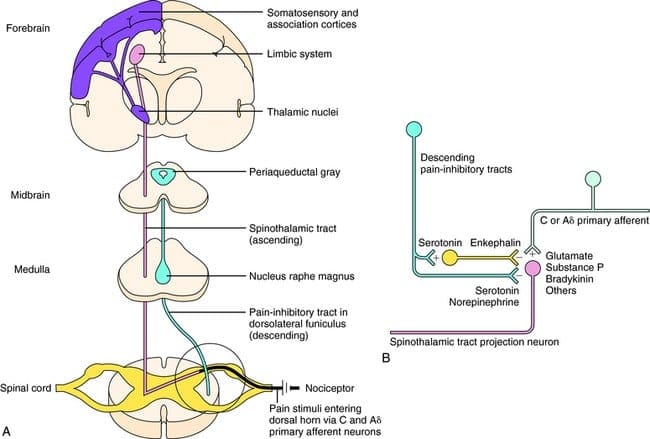
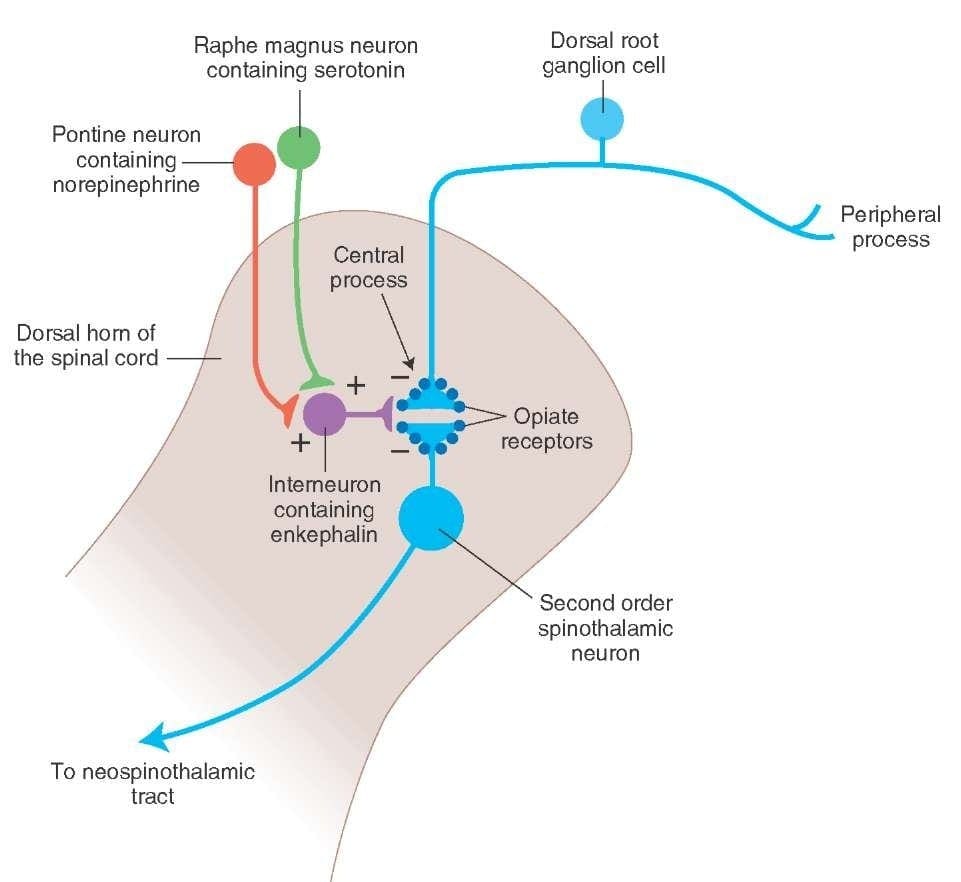
O que ativa o PAG para exercer suas conseqüências? Descobriu-se que a estimulação nociva desencadeia neurônios no núcleo reticular gigantocellularis, ou RGC. O núcleo Rgc inerva tanto o PAG quanto o NRM. O PAG envia axônios para o NRM, e os nervos no NRM enviam seus axônios para a medula espinhal. Além disso, lesões do funículo dorsolateral bilateral, ou DLF, denominadas DLFX, bloqueiam a analgesia produzida tanto pela estimulação elétrica quanto pela microinjeção de opiáceos diretamente na PAG e NRM, mas apenas atenuam os efeitos analgésicos sistêmicos dos opiáceos. Estas observações suportam a hipótese de que as vias descendentes discretas do DLF são necessárias para OA e SPA.
O DLF é composto de fibras originárias de vários núcleos do tronco cerebral, que podem ser serotoninérgicos, ou 5-HT, de nervos localizados dentro do núcleo magno da rafe, ou NRM; neurônios dopaminérgicos originários da área tegmentar ventral, ou VTA, e neurônios adrenérgicos originários do locus coeruleus, ou LC. Essas fibras descendentes suprimem a entrada nociva nos neurônios nociceptivos da medula espinal nas lâminas I, II e V.
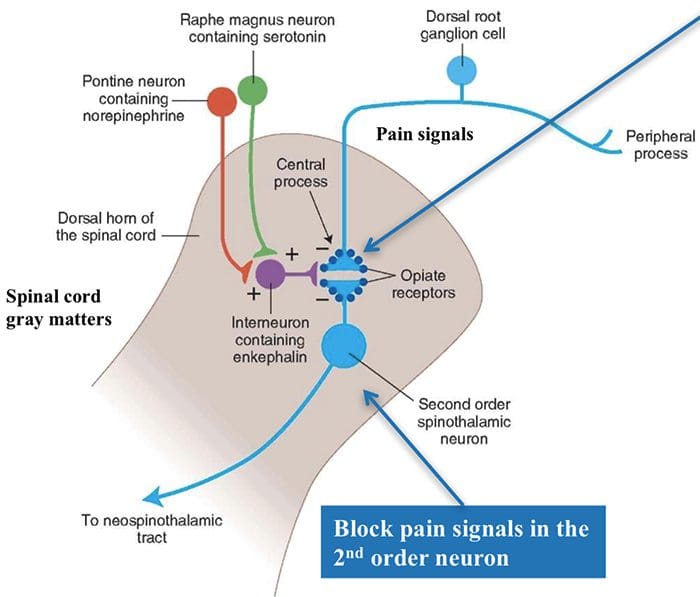
Os receptores opióides também foram descobertos no corno dorsal da medula espinhal, principalmente nas lâminas Rexed I, II e V, e tais receptores espinais opiáceos mediam os efeitos inibitórios nos neurônios do corno dorsal, transmitindo informações nociceptivas. A ação da morfina parece ser exercida igualmente nos núcleos da medula espinal e do tronco cerebral, incluindo o PAG e o NRM. A morfina sistêmica atua tanto no receptor do encéfalo quanto na medula espinhal para produzir analgesia. A morfina se liga aos receptores opióides do tronco encefálico, que desencadeiam a via serotoninérgica descendente do tronco encefálico na medula espinhal, bem como o DLF, e estes têm uma sinapse mediada por opióides no nível da medula espinhal.
Esta observação demonstra que estímulos nocivos, em vez de estímulos não nocivos, determinam a teoria do controle da comporta, que são críticos para a ativação do circuito de modulação da dor descendente, onde a dor inibe a dor pela via descendente do DLF. Além disso, há conexões ascendentes no PAG e nos núcleos da rafe no complexo PF-CM. Essas regiões talâmicas fazem parte da modulação da dor ascendente no grau diencéfalo.
Analgesia Induzida por Estresse (SIA)
A analgesia pode ser produzida em certas circunstâncias estressantes. A exposição a muitos eventos estressantes ou dolorosos diferentes gera uma resposta analgésica. Este fenômeno é conhecido como analgesia induzida por estresse, ou SIA. Acredita-se que a analgesia induzida pelo estresse forneça informações sobre os fatores fisiológicos e psicológicos que desencadeiam o controle endógeno da dor e os sistemas de opiáceos. Por exemplo, soldados feridos em uma batalha ou atletas machucados em esportes às vezes relatam que não sentem dor ou desconforto durante a batalha ou o jogo, no entanto, eles vão passar pela dor depois que a situação específica parar. Tem sido demonstrado em animais que choques elétricos causam analgesia induzida por estresse. Com base nesses experimentos, supõe-se que a pressão exercida pelos soldados e pelos atletas tenha suprimido a dor que eles experimentariam mais tarde.
Acredita-se que os opiáceos endógenos são produzidos em resposta ao estresse e inibem a dor, desencadeando o sistema descendente do mesencéfalo. Além disso, alguns SIA exibiram tolerância cruzada com analgesia por opiáceos, o que indica que esta SIA é mediada por receptores de opiáceos. Experiências utilizando diferentes parâmetros de estimulação de choque elétrico demonstram tal analgesia induzida por estresse e algumas daquelas ansiedades que produzem analgesia poderiam ser bloqueadas pelo antagonista opioide naloxona, enquanto outras não foram bloqueadas pela naloxona. Em conclusão, estas observações levam à decisão de que existem formas opiáceos e não opiáceas da AIS.
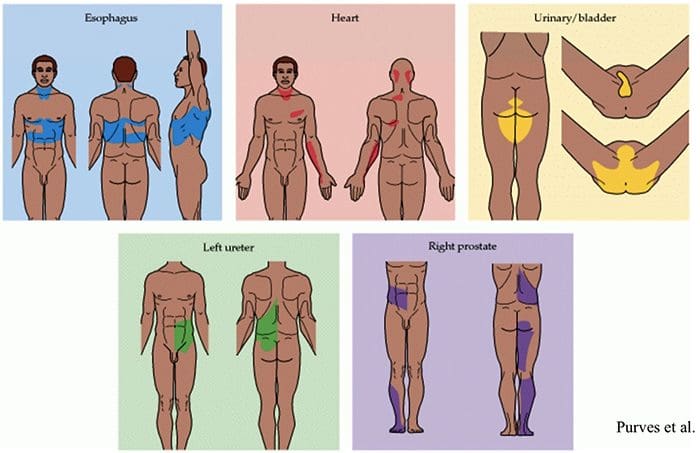
Reflexo somatovisceral
O reflexo somatovisceral é um reflexo no qual as funções viscerais são ativadas ou inibidas pela estimulação sensorial somática. Em animais experimentais, a estimulação nociva e inócua de aferentes somáticos provou provocar mudanças reflexas na atividade eferente simpática e, conseqüentemente, na função do órgão efetor. Estes fenômenos foram mostrados em regiões como o trato gastrointestinal, trato urinário, medula supra-renal, células linfáticas, coração e vasos do cérebro e nervos periféricos.
Mais freqüentemente, as incisões são provocadas experimentalmente pela estimulação de aferências cutâneas, embora alguns trabalhos também tenham sido realizados em aferências musculares e articulares, incluindo aquelas de células espinhais. As respostas finais representarão a integração de múltiplas influências tônicas e reflexas e poderão exibir tendências de lateralidade e segmentação, bem como excitabilidade variável em linha com os aferentes envolvidos. Dada a complexidade e multiplicidade de mecanismos envolvidos na última expressão da resposta reflexa, as tentativas de extrapolar para situações clínicas devem ser mais provavelmente conduzidas em favor de estudos fisiológicos sistemáticos adicionais.
O escopo de nossa informação é limitado a quiropraxia, bem como lesões e condições da coluna vertebral. Para discutir o assunto, sinta-se à vontade para perguntar ao Dr. Jimenez ou entrar em contato conosco 915-850-0900 .
Curated pelo Dr. Alex Jimenez
Tópicos Adicionais: Ciática
A ciática é medicamente referido como uma coleção de sintomas, em vez de uma única lesão e / ou condição. Os sintomas da dor do nervo ciático, ou ciática, podem variar em frequência e intensidade, no entanto, é mais comumente descrita como uma dor súbita, aguda (tipo faca) ou elétrica que irradia da parte inferior das costas para as nádegas, quadris, coxas e pernas no pé. Outros sintomas da ciática podem incluir, sensação de formigamento ou queimação, dormência e fraqueza ao longo do comprimento do nervo ciático. Ciática mais freqüentemente afeta indivíduos entre as idades de 30 e 50 anos. Pode desenvolver-se frequentemente como resultado da degeneração da espinha devido à idade, no entanto, a compressão e irritação do nervo ciático causada por um abaulamento ou hérnia de disco, entre outros problemas de saúde da coluna vertebral, também pode causar dor no nervo ciático.

TÓPICO EXTRA IMPORTANTE: Chiropractor Ciática Sintomas



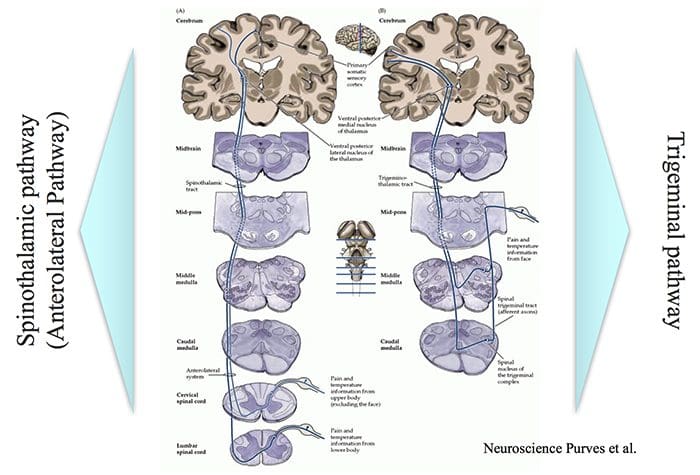
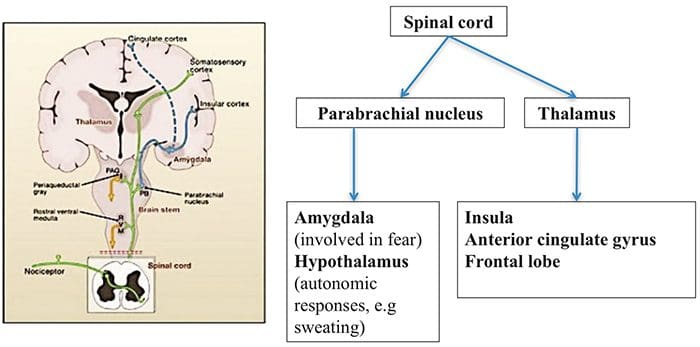 Áreas do cérebro envolvidas no processamento de sinais nociceptivos
Áreas do cérebro envolvidas no processamento de sinais nociceptivos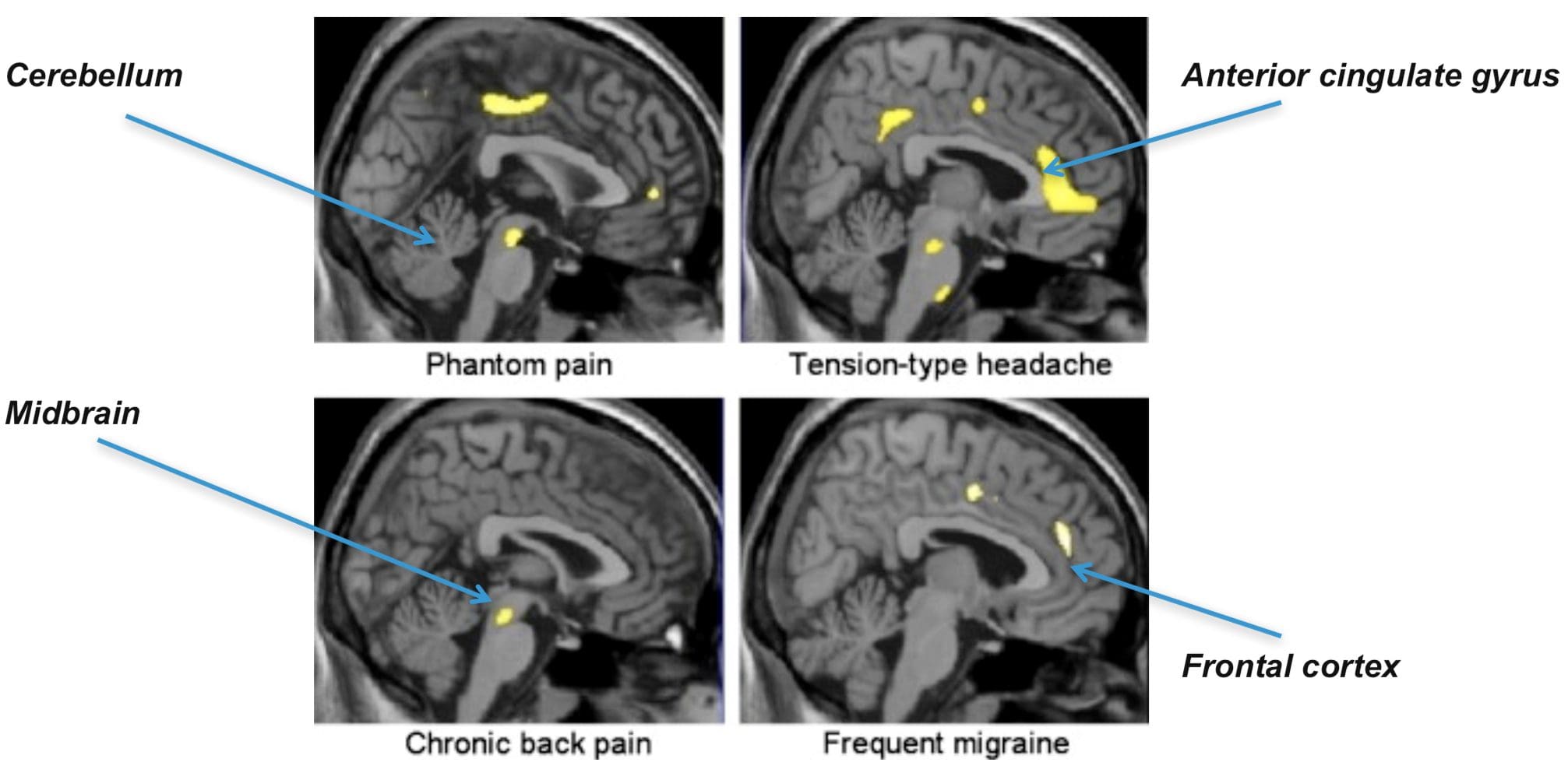 O cíngulo anterior e o córtex da ínsula são ativados em seres humanos
O cíngulo anterior e o córtex da ínsula são ativados em seres humanos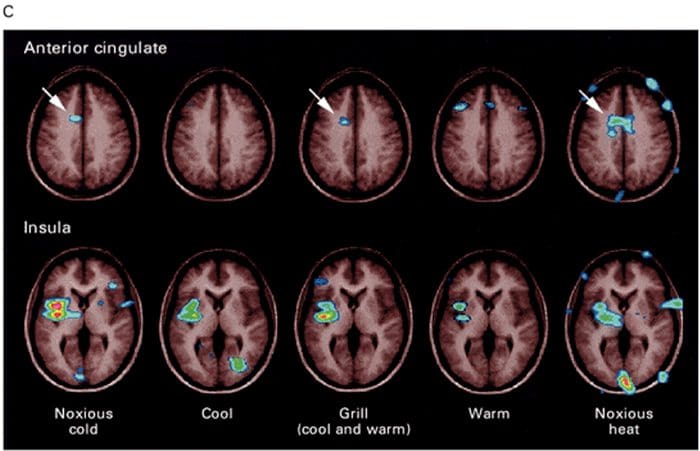
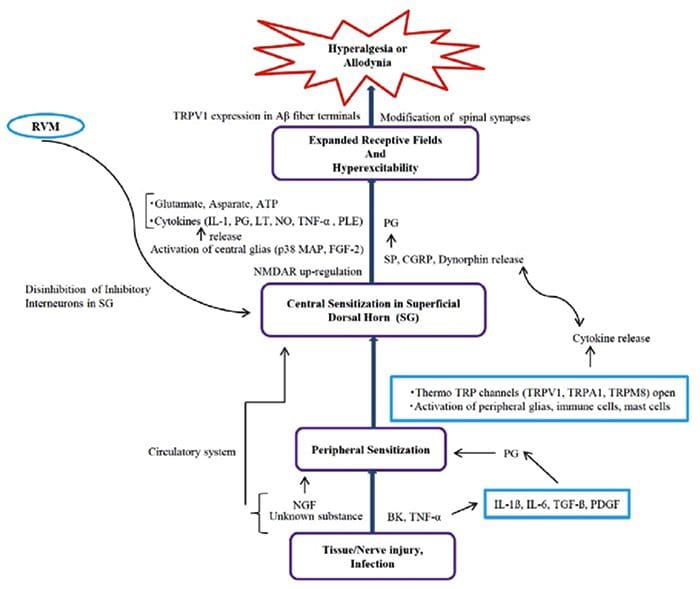
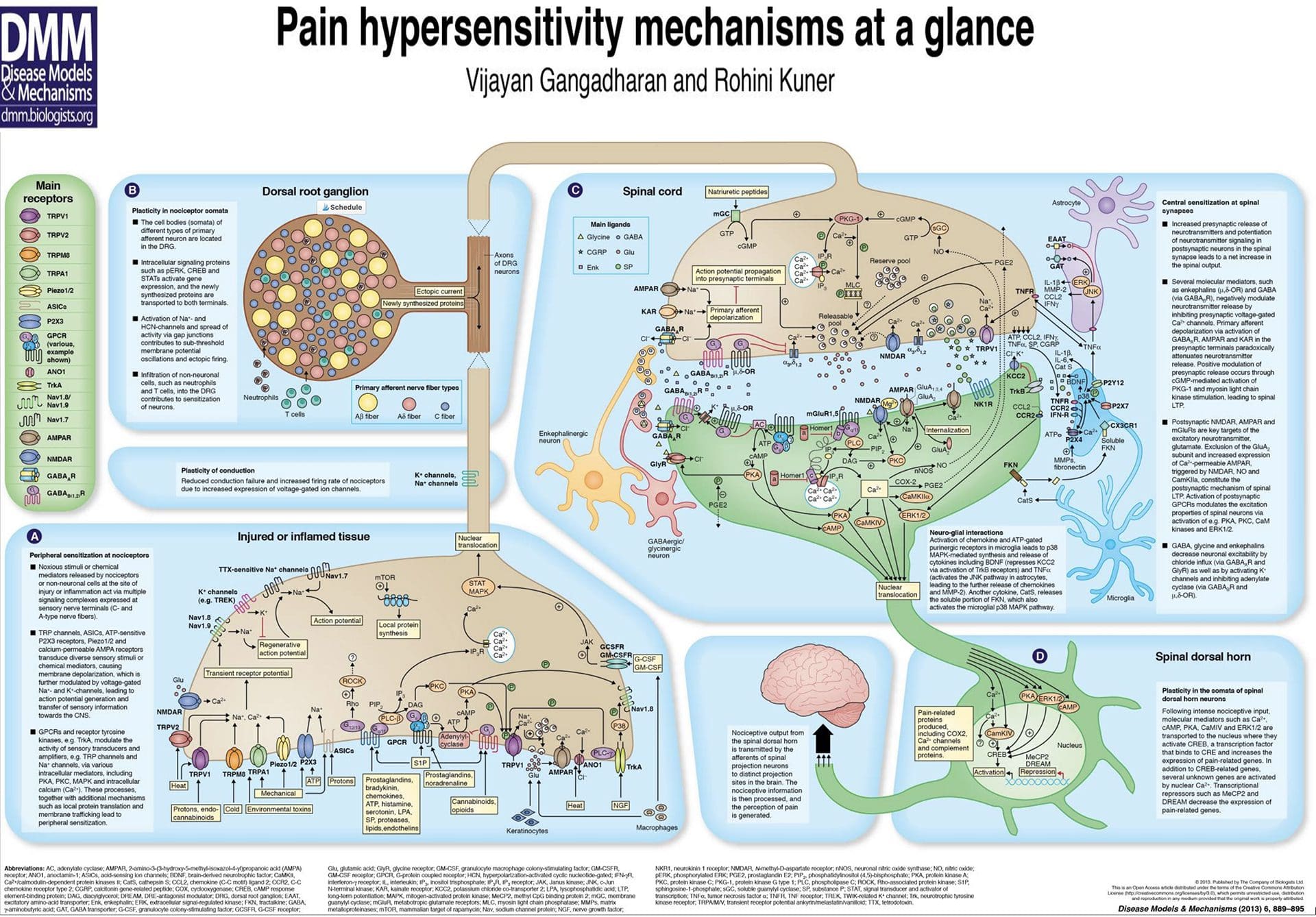
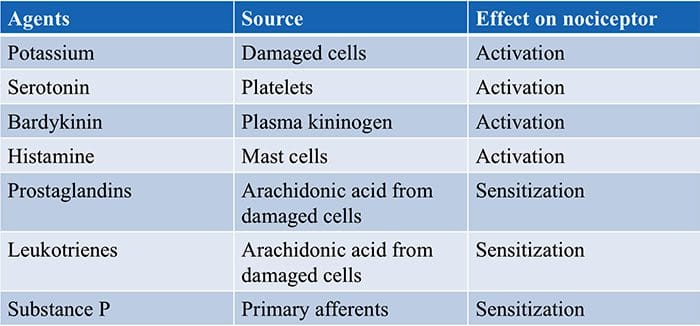
 Sopa Inflamatória - Hiperalgesia
Sopa Inflamatória - Hiperalgesia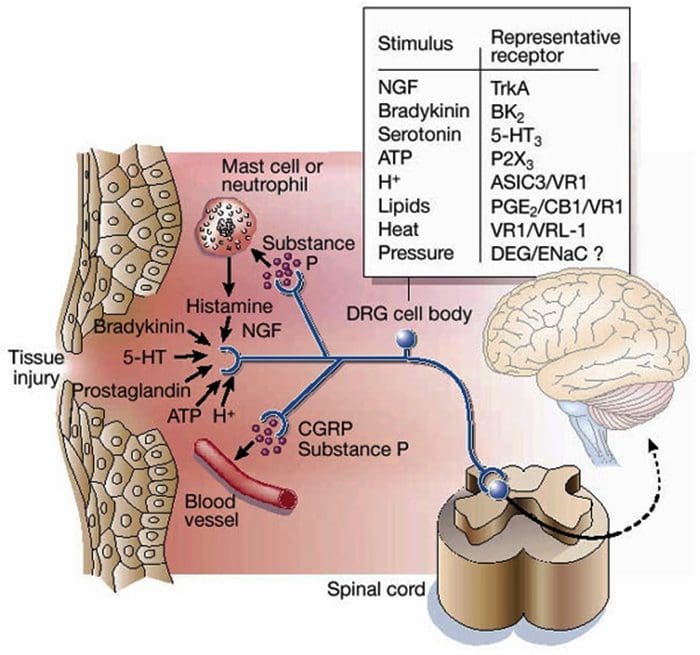
 Teoria do Controle do Portão da Dor
Teoria do Controle do Portão da Dor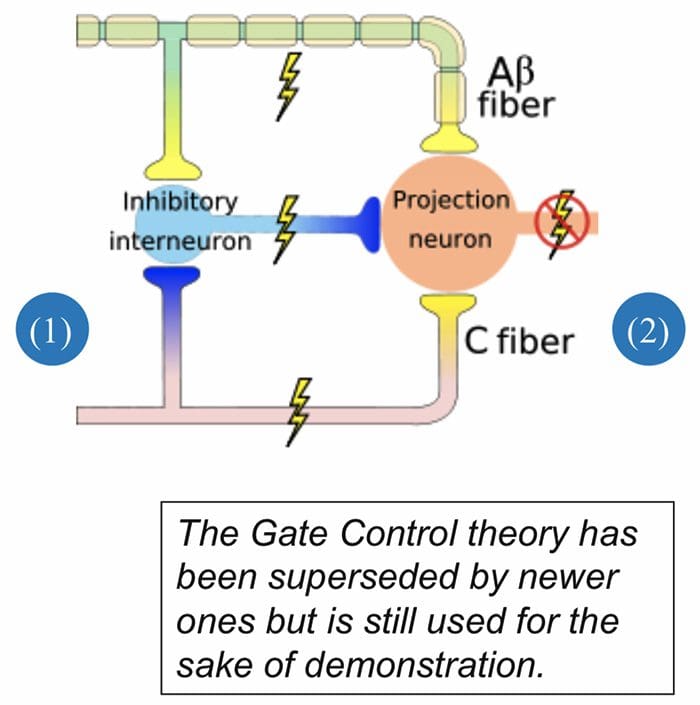
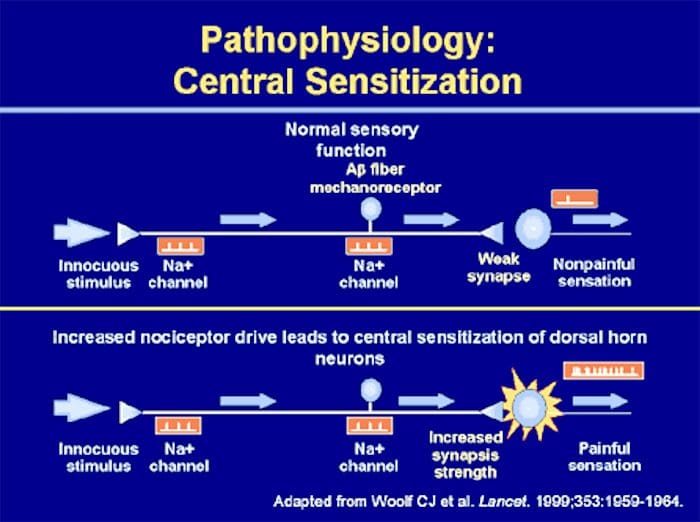
 Anormalidades do sistema de dor
Anormalidades do sistema de dor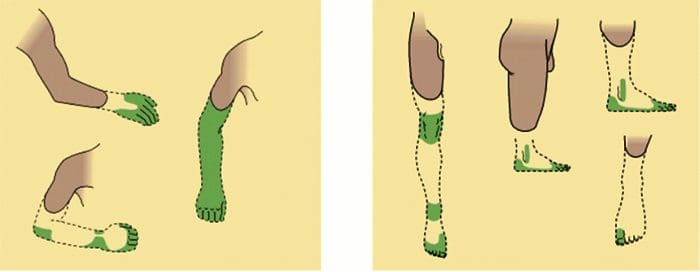 Sensibilização Periférica
Sensibilização Periférica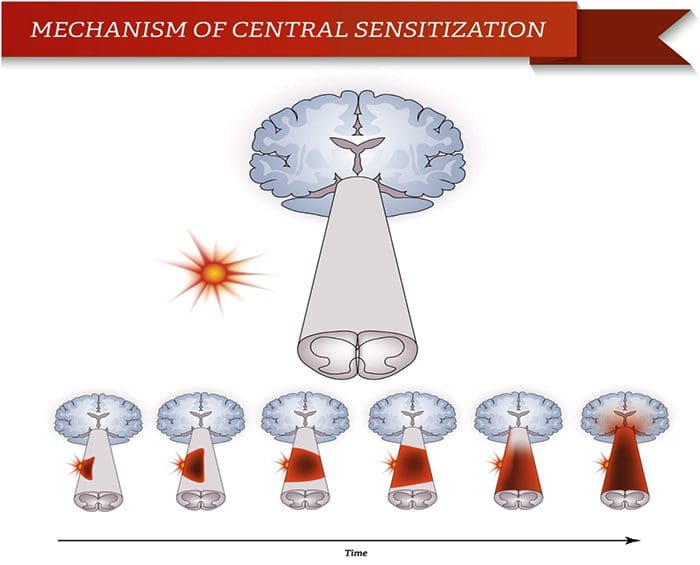
 Organização do córtex somatossensorial
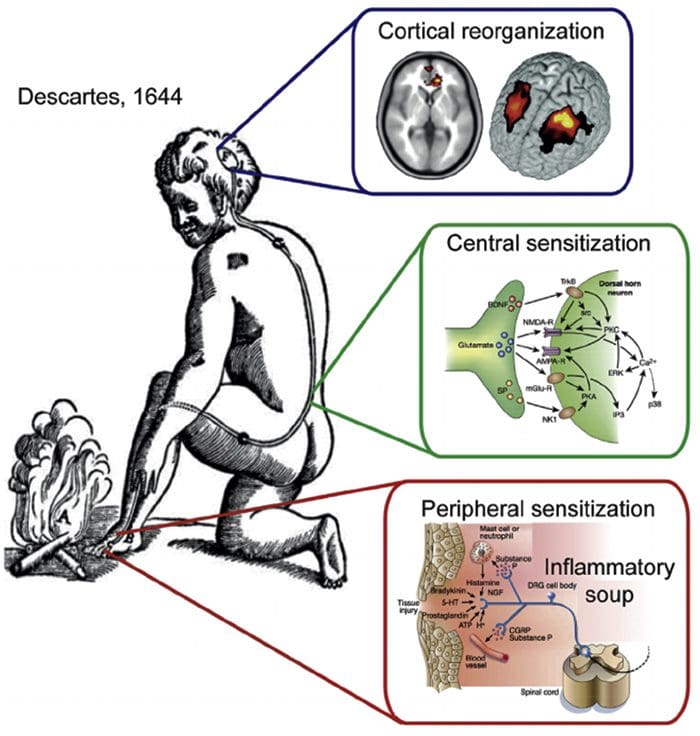
Organização do córtex somatossensorial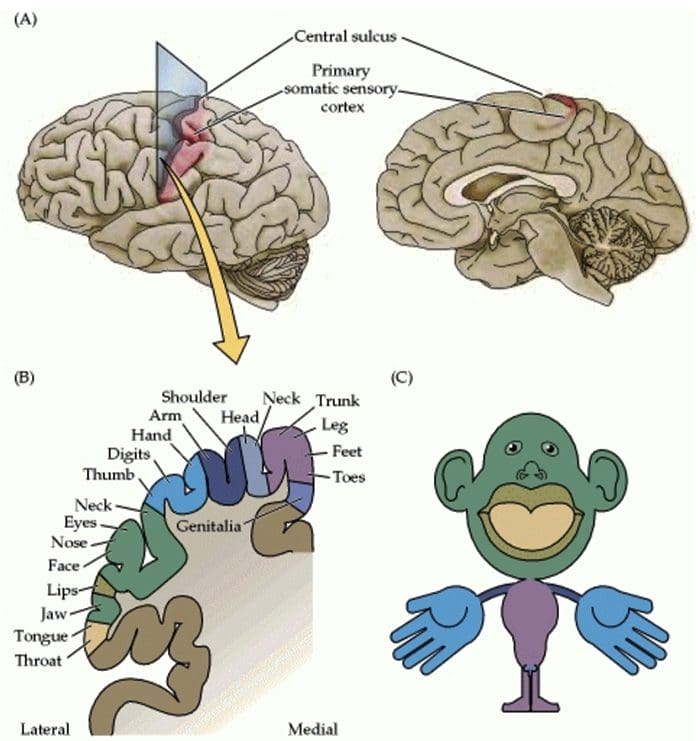 Reorganização Cortical
Reorganização Cortical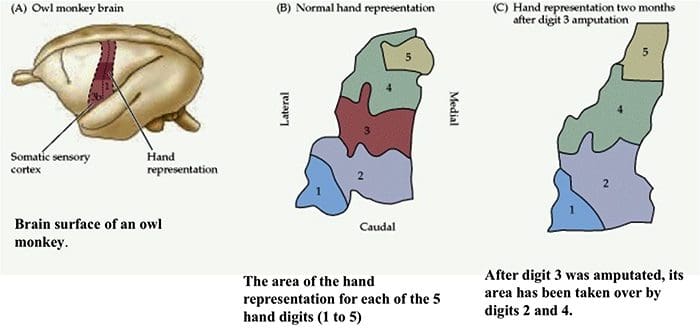

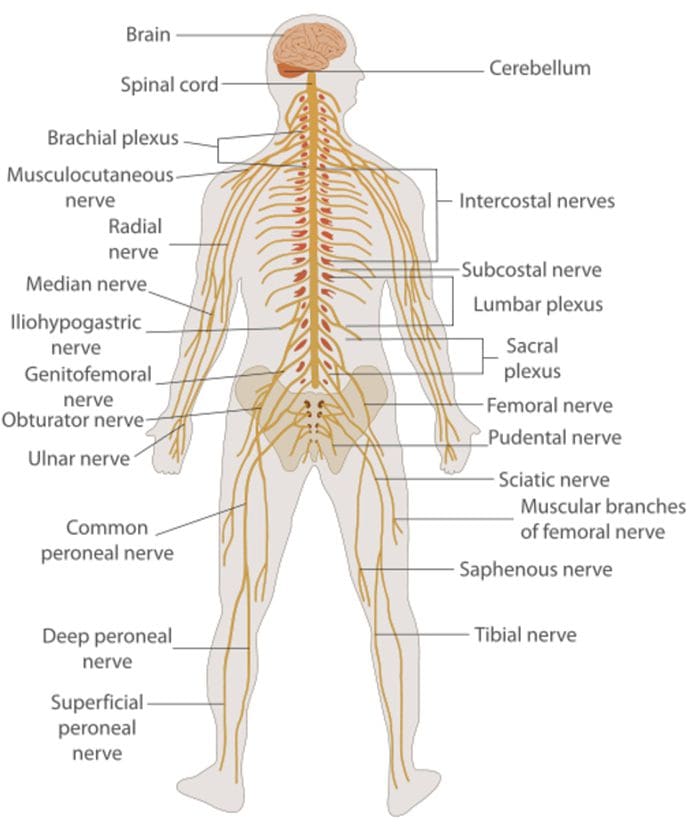
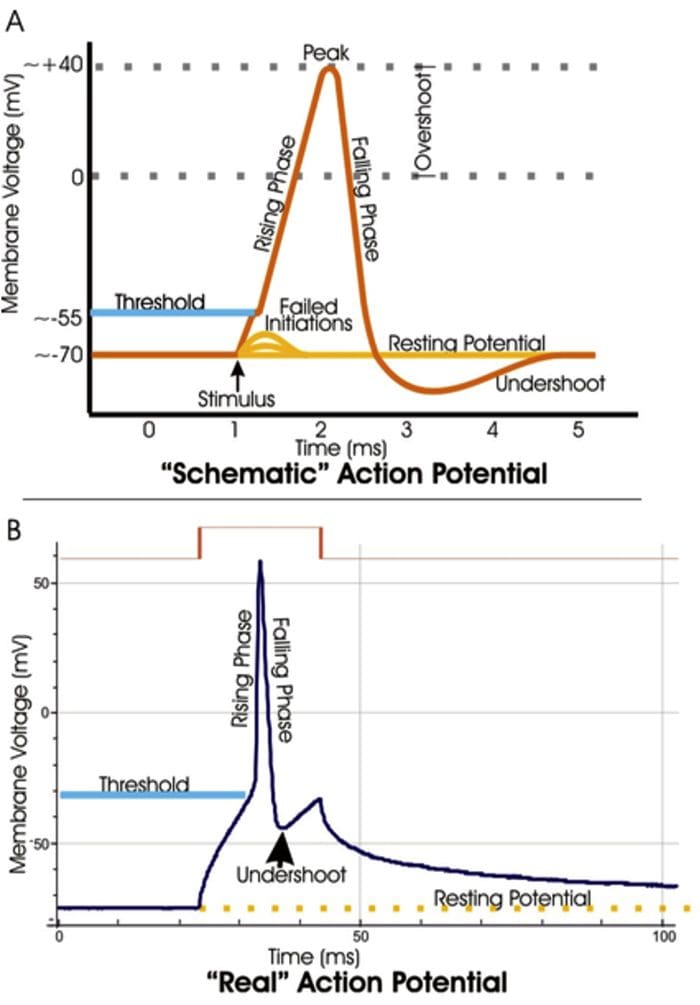
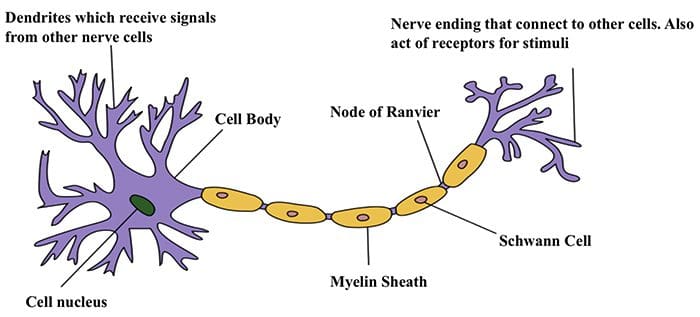 Comunicação Celular Nervo Celular a Nervo
Comunicação Celular Nervo Celular a Nervo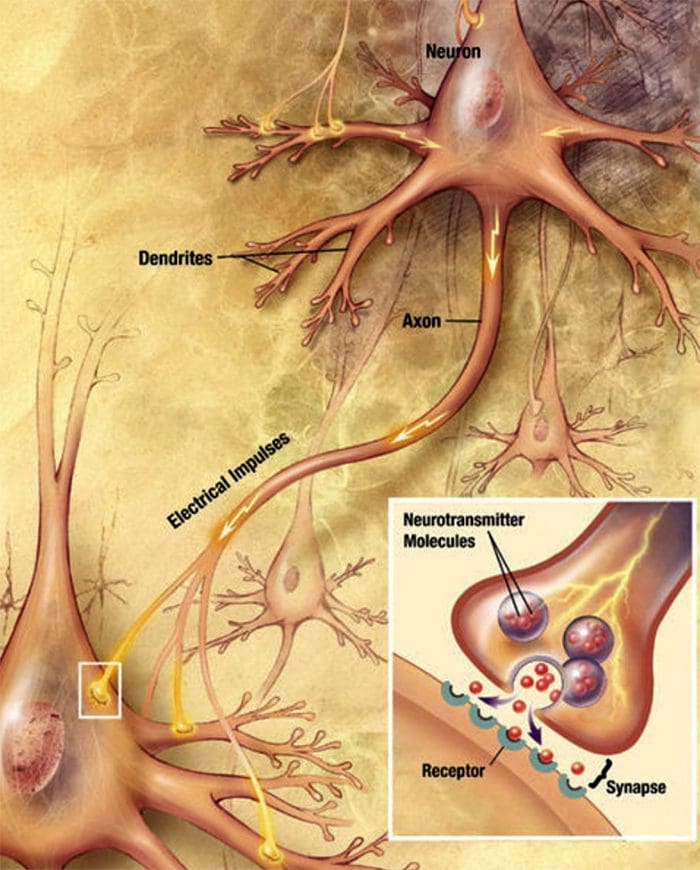 As células nervosas se comunicam com outras células liberando uma substância química das terminações nervosas Neurotransmissores
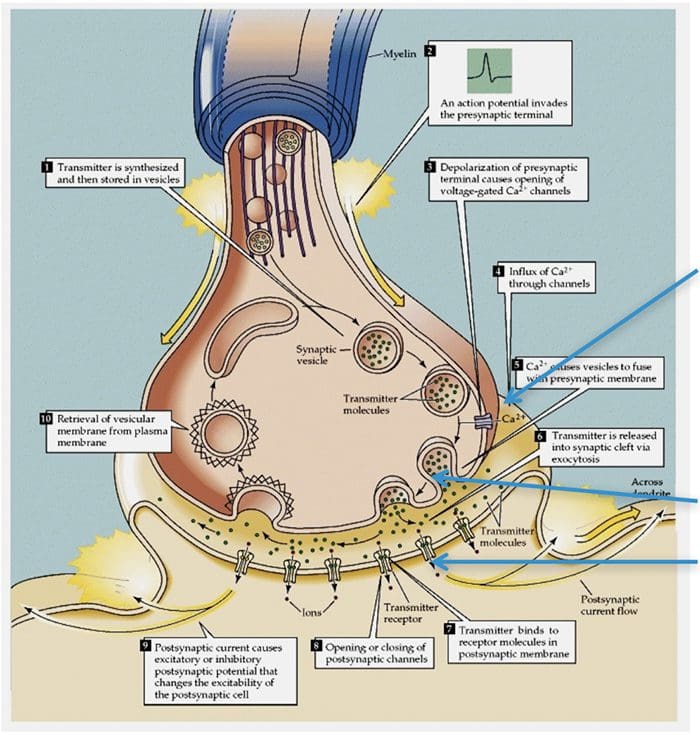
As células nervosas se comunicam com outras células liberando uma substância química das terminações nervosas Neurotransmissores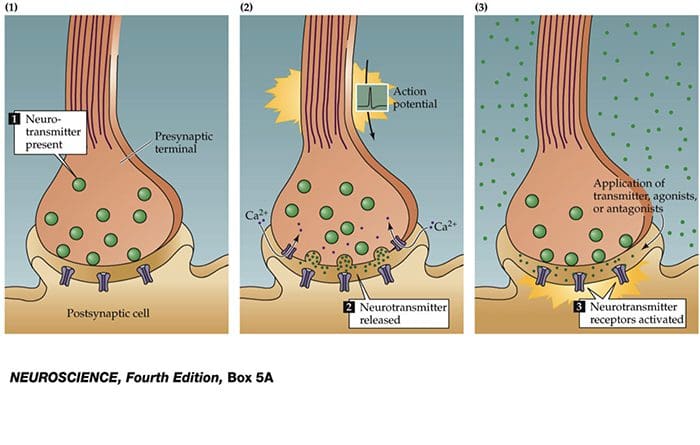
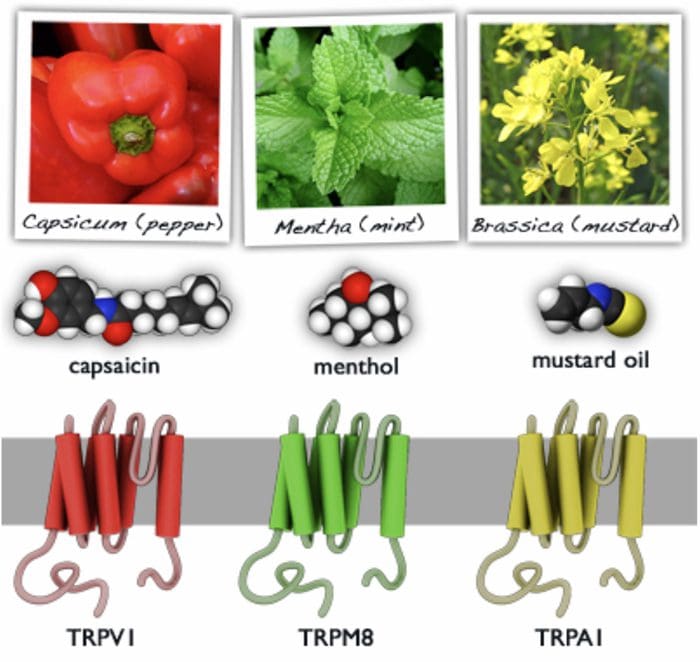
 Canais TRP
Canais TRP